Asociación entre biomarcadores en tomografía de coherencia óptica y agudeza visual en pacientes con edema macular diabético tratados con antiangiogénicos
Dres. Camila Iris Dorrego MDa; Silvana Pellice MDa; Ana Lisa Carauni MDa; Luciana Chiapella PhDb; Gimena Dapena MDa; Pablo Chamartin MDa; Franco Daniel Rocco MDa; Arturo Alberto Alezzandrini MD PhD c
a Sanatorio Otamendi y Miroli, Universidad de Buenos Aires, Buenos Aires, Argentina.
b Facultad de Ciencias Bioquímicas y Farmacéuticas, Universidad Nacional de Rosario - CONICET, Argentina.
c Oftalmos Centro Oftalmológico de Alta Complejidad, Universidad de Buenos Aires, Buenos Aires, Argentina.
Dra. Camila Iris Dorrego
camiladorrego@hotmail.com
Recibido: 23/8/2021
Aceptado: 11/10/2021
Disponible en www.sao.org.ar
Arch. Argent. Oftalmol. 2021; 19: 11-23
RESUMEN
Objetivos:
Evaluar la asociación entre los principales biomarcadores del Edema Macular Diabético (EMD) y la Agudeza Visual (AV), y determinar su importancia como herramienta pronóstica a la hora de iniciar un tratamiento antiangiogénico en cada paciente.
Métodos: Estudio de cohorte retrospectivo, observacional y longitudinal. Se analizaron 25 escaneos de OCT de 23 pacientes con edema macular diabético (EMD) y se registró la Agudeza Visual Mejor Corregida (AVMC) al inicio, y a los 3, 6 y 9 meses de tratamiento. Las imágenes basales se evaluaron para el tipo predominante de edema macular (Cistoide, espongiforme, con desprendimiento seroso subfoveal o con compromiso traccional); presencia de daño en la retina externa (considerado como cualquier discontinuidad en la Membrana Limitante Externa, Zona Elipsoide y/o Zona de Interdigitación); presencia de desorganización de las Capas Internas de la Retina (DRIL) y cantidad de Puntos Hiperreflectivos (PH) así como del Espesor Macular Central (EMC). Las correlaciones entre cada biomarcador y la ganancia de Agudeza Visual se analizaron utilizando modelos longitudinales de efectos mixtos.
Resultados:
Se incluyeron veinticinco ojos con EMD NAIVE de tratamiento. La AVMC basal se encontraba entre 0,3 y 1,3 en un logaritmo del gráfico visual de ángulo mínimo de resolución (LogMAR). El tipo de edema macular, la presencia de DRIL y el EMC presentaron un efecto estadísticamente significativo sobre la modificación de la AV a lo largo del tiempo (p< 0,001 en todos los casos). Los pacientes con DRIL mostraron menor ganancia de AV en términos LogMAR a los 9 meses que los pacientes sin DRIL, siendo la diferencia estadísticamente significativa (p=0,026), y mostraron menor mejoría en la AV a lo largo de los nueve meses de tratamiento (efecto de interacción p=0,007). Los subtipos de edema con desprendimiento seroso subfoveal, y con componente traccional por otro lado, ganaron menos visión que los pacientes que sólo presentaban edema macular de tipo cistoide. No hubo diferencias estadísticamente significativas entre la presencia de PH y la alteración de las capas retinianas externas con la AV a lo largo del tiempo de tratamiento.
Conclusión: Es de gran utilidad evaluar el EMC inicial, aunque no de manera aislada, así como es primordial evaluar y considerar la presencia de DRIL como biomarcador pronóstico, que en el presente estudio resultó ser el aquel con mayor potencial como predictor de respuesta clínica en términos de AV.
Palabras clave: Edema macular diabético, biomarcadores, OCT, DRIL.
ABSTRACT
Purpose:
To evaluate the association between the main biomarkers of Diabetic Macular Edema (DME) and the Visual Acuity (VA), and determine its importance as a prognostic tool at time to start an antiangiogenic treatment in each patient.
Methods: Retrospective, observational and longitudinal cohort study. 25 OCT scans of 23 patients with diabetic macular edema (DME) were analyzed, and the Best Corrected Visual Acuity (BCVA) at baseline and at 3, 6 and 9 months of treatment was registered. Baseline images were evaluated for predominant type of macular edema (cystoid, spongiform, with subfoveal serous detachment, or tractional compromise); presence of outer retinal damage (ORD, considered as any discontinuity in Limiting Extern Membrane, Ellipsoid Zone, and/or Interdigitation Zone); presence of disorganization of the Inner Retinal Layers (DRIL), and Hyperreflective Focis (HF) quantity, as well as Central Macular Thickness (CMT). Correlations between each OCT biomarker and visual acuity gain were analyzed using longitudinal mixed-effects models.
Results:
Twentyfive eyes with NAIVE DME were included. Baseline best-corrected visual acuity (BCVA) was between 0.3 and 1.3 on a logarithm of minimum angle of resolution visual chart (logMAR). Type of macular edema, DRIL presence, and CMT presented a statistically significant effect on the VA modification along the time (p<0,001 in all cases). Patients with DRIL showed worse VA in logMAR terms at 9 months than patients without DRIL, being the difference statistically different (p=0,026), and showed less improvement in VA along the nine months treatment (interaction effect p=0,007). Eyes with subfoveal serous detachment and eyes with tractional component gained less vision than patients with only cystoid macular edema. There were no statistically significant differences between presence of hyperreflective focis, extern retinal layers alteration and VA along the treatment time.
Conclusion:
This study showed that it is useful to assess the initial CMT but not in isolation, and above all the presence of DRIL, which proved to be the tomographic biomarker with the greatest potential as a predictor of clinical response in terms of VA.
Key words: Diabetic macular edema, OCT, biomarkers, DRIL.
INTRODUCCIÓN
El Edema Macular Diabético (EMD) representa una acumulación de líquido dentro de la porción central de la retina, que surge como consecuencia de la falla de la barrera hematorretiniana y sigue siendo una causa importante de pérdida visual en pacientes con diabetes mellitus.1 La clasificación del EMD es importante para establecer la gravedad de la patología, así como para seleccionar el tratamiento más adecuado para el paciente. Han sido descritos diferentes patrones de edema macular hasta la fecha: el edema espongiforme está presente en el 88% al 96% de todos los EMD. Es una fuga de líquido en las capas más externas de la retina, y si se presenta de forma aislada, tiene una buena respuesta al tratamiento. El de tipo cistoide está presente en 47% a 57% de todos los EMD; son cambios quísticos intrarretinianos y representan formas más graves de fuga asociada a peor AV; el tratamiento con láser en estos casos es menos eficaz, pero tienen buena respuesta al tratamiento farmacológico. El edema macular traccional ocurre en el 15% de todos los EMD, no responde a la terapia con láser o al tratamiento farmacológico aislado, y requiere vitrectomía. 2, 3
Por su parte, el desprendimiento seroso subfoveal (DSS) tiene una incidencia del 11% al 15% en los EMD; la terapia láser se ha mostrado ineficaz en estos casos y se ha propuesto la existencia de un componente inflamatorio asociado que podría explicar una mejor respuesta a los esteroides.3, 4
Sin embargo, a pesar de estas asociaciones, en los últimos años, los avances en la tecnología de la OCT han permitido ampliar el estudio del EMD para centrarse en otros biomarcadores que con frecuencia lo acompañan. Se ha demostrado que éstos se relacionan en diferentes medidas con la estructura y respuesta terapéutica funcional. Los más estudiados incluyen: alteraciones de las capas externas de la retina, desorganización de las capas internas de la misma (signo conocido en los últimos años como “DRIL”), la presencia de puntos hiperreflectivos (PH) en las capas internas o externas de la retina, y también el espesor macular central (EMC), siendo uno de los primeros en ser estudiados en relación a la agudeza visual, mostrando resultados contradictorios, lo que condujo a la necesidad de encontrar parámetros más confiables al hablar con el paciente de un pronóstico visual.
Los biomarcadores encontrados en la OCT nos ayudan a identificar alteraciones ultraestructurales en etapas tempranas de la enfermedad. Su presencia se ha relacionado con la gravedad de la retinopatía diabética, lo que los hace útiles para plantear un pronóstico y evaluar la respuesta a la terapia. Es importante destacar que se están estudiando nuevos biomarcadores, como el índice de vascularización coroidea en OCT, anomalías vasculares periféricas en la angiografía de campo amplio, o en la angiografía por OCT, donde se evalúa la zona avascular foveal (FAZ) o la dimensión fractal. La utilidad de estas técnicas es que podrían detectar enfermedades subclínicas y cambios vasculares de la retina incluso antes de producirse cambios clínicamente detectables o el desarrollo de síntomas visuales.8
MATERIALES Y MÉTODOS
El estudio fue designado como de cohorte, retrospectivo, observacional y longitudinal. Veintitrés pacientes (25 ojos) afectados por EMD referidos al Departamento de Retina del Instituto de Alta Complejidad Oftalmos, desde noviembre de 2018 a julio de 2019, fueron considerados para el estudio.
Para ser incluidos en el análisis, los pacientes debían cumplir con los siguientes criterios: (1) edad entre 24 a 84 años; (2) diabetes mellitus tipo 1 o 2; (3) y EMD naïve, que ocasione pérdida visual (edema macular clínicamente definido, y por un espesor macular central EMC >250 micras, así como fluido intra o subretinal en la SD-OCT).
Todos los pacientes recibieron un tratamiento mensual con un antiangiogénico intravítreo en un lapso de nueve meses. Para pacientes que recibieron un tratamiento bilateral, ambos ojos fueron incluidos (dos pacientes).
Los criterios de exclusión fueron: cualquier otra patología oftalmológica que provoque opacidad significativa, como una catarata densa o hemorragia vítrea, pobre calidad de imágenes por OCT, inhabilidad del paciente para colaborar con la examinación o la adquisición de imágenes de OCT, así como cualquier terapia previa recibida para el EMD.
Se analizaron veinticinco escaneos de OCT de 23 pacientes con EMD y su Agudeza Visual Mejor Corregida (AVMC) al inicio y a los 3, 6 y 9 meses de tratamiento.
La AVMC inicial de los pacientes se encontraba entre 0,3 y 1,3 en unidades logMAR.
Se evaluaron imágenes basales para determinar el tipo predominante de edema macular (cistoide, espongiforme, con desprendimiento seroso subfoveal o de tipo traccional), así como la presencia de biomarcadores como alteraciones en la retina externa (incluyendo aquí aquellos con discontinuidad de la membrana limitante externa, de la zona elipsoide y/o de la zona de interdigitaciones en el área macular), la presencia de DRIL, y la cantidad de PH, así como el EMC (Fig. 1). La correlación entre cada biomarcador y la ganancia de agudeza visual se analizó utilizando modelos longitudinales de efectos mixtos. Cada paciente se sometió a un examen oftalmológico, que incluyó la AVMC medida en unidades logMAR, biomicroscopía con lámpara de hendidura y OCT de dominio espectral (SD-OCT; HRA Heidelberg, Alemania).
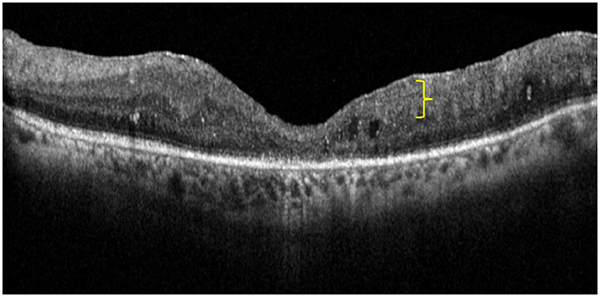
Figura 1: Presencia concomitante de DRIL y alteración de la retina externa en el área subfoveal en un paciente con EMD de predominio espongiforme. (DRIL: llave amarilla)
Análisis estadístico
Para representar la distribución de la AVMC de los 25 ojos en los cuatro momentos de medición, según el tipo de edema y la presencia o ausencia de los biomarcadores en estudio, se utilizaron diagramas de caja y bigotes. Para evaluar la posible diferencia en la AVMC media entre los grupos en cada momento de medición, se realizó un análisis ANOVA.
Para analizar la evolución temporal de la AVMC según el tipo de edema y la presencia o ausencia de los biomarcadores, se ajustaron modelos longitudinales univariados con efectos mixtos, considerando como efectos fijos el tiempo de tratamiento, la covariable a estudiar y la interacción entre ellos y, como efectos aleatorios anidado, los pacientes y los ojos. Para evaluar la significación de los efectos fijos, se calculó la probabilidad asociada al test tipo II de Wald y se estimaron los coeficientes del modelo. Se calculó el valor de criterio de información de Akaike (AIC), a fin de comparar el ajuste de los datos según la covariable considerada.
Posteriormente, se ajustó un modelo longitudinal de efectos mixtos multivariado, incluyendo todos los biomarcadores, ajustado por tipo de edema. Se empleó el algoritmo de eliminación hacia atrás según el valor de AIC para obtener un conjunto de covariables explicativas de la evolución temporal de la AVMC.
En todos los casos, se consideró significativa una probabilidad asociada p menor a 0.05. El análisis se llevó a cabo con el software R v.3.6.2 y RStudio v. 1.2.5033.
RESULTADOS
Tipo de edema
Al comparar la AVMC media en cada momento de medición, según el tipo de edema macular diabético, no se encontraron diferencias estadísticamente significativas en ninguno de dichos momentos (Fig. 2).
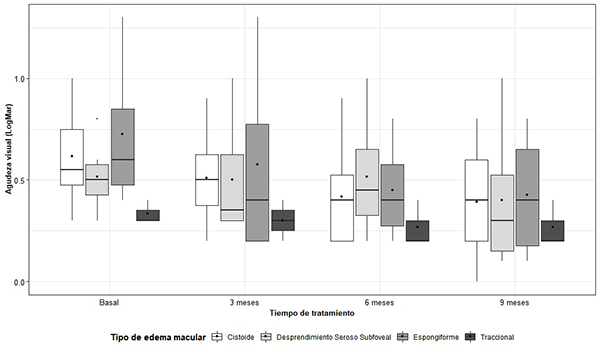
Figura 2: Distribución de la AV (logMar) de acuerdo al tiempo de medición y tipo de edema
DRIL
La agudeza visual media no resultó estadísticamente distinta según presencia o ausencia de DRIL en las tres primeras mediciones. Sin embargo, se encontró una diferencia significativa al comparar ambos grupos a los 9 meses (p=0.026), dado que los casos con presencia de DRIL mostraron un valor medio de LogMar mayor a aquellos con ausencia de DRIL (Figura 3).
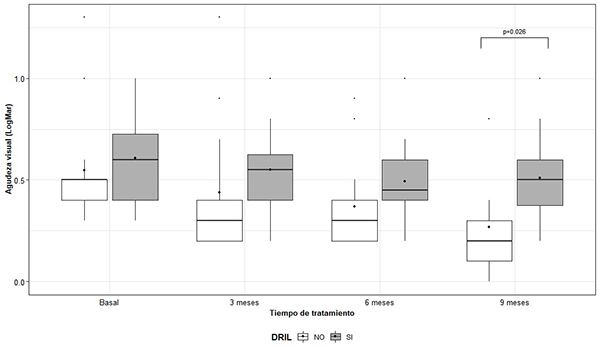
Figura 3: Distribución de la AV (LogMar) de acuerdo al tiempo de medición y presencia de DRIL.
Al considerar la modificación longitudinal de la agudeza visual, se encontró que la misma resultó significativa en función del tiempo (p < 0.001) y de la presencia de DRIL (efecto interacción: p=0.007). Los casos con DRIL presentaron un menor decremento en la agudeza visual que los casos sin DRIL (Tabla 1).
Alteración de la retina externa
La agudeza visual media resultó estadísticamente diferente entre los casos con alteración de la retina externa y los casos sin ésta, cuando se midió a los 6 meses de tratamiento (p=0.035). (Fig. 4). No se encontraron diferencias significativas en los otros momentos de medición (Fig. 5). Al analizar el comportamiento de la agudeza visual, según escala LogMar, en forma longitudinal, se encontró que la misma presentó un decrecimiento estadísticamente significativo en función del tiempo de tratamiento (p < 0.001), sin diferir de acuerdo la presencia o ausencia de alteraciones en la retina externa (efecto interacción: p=0.912) (Tabla 1).
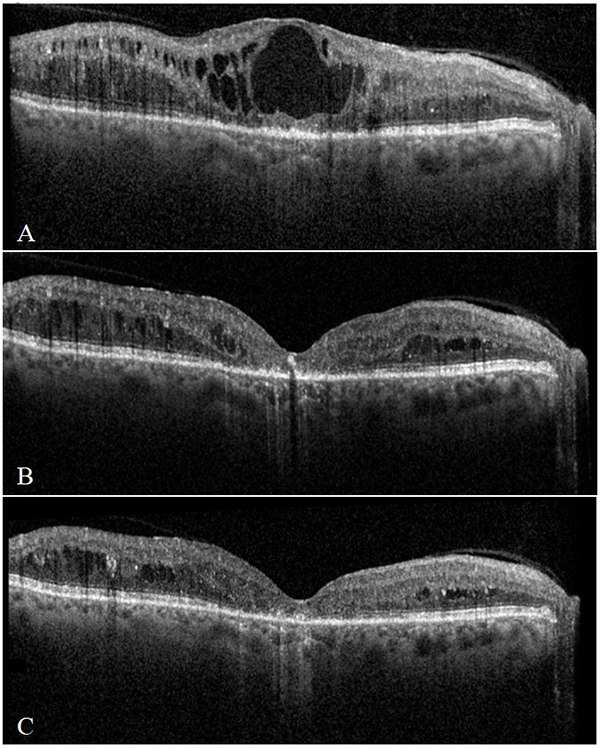
Figura 4: Tomografía de Coherencia Óptica: signos en presencia de EMD. EMD cistoide con alteración en las capas de la retina externa y pobre ganancia de AV a pesar de una marcada reducción del EM a los nueve meses de tratamiento. AVMC: A) Línea de base: LogMAR 0,9 (Eq. Snellen: 20/160); B) Mes 3: LogMAR 0,7 (Eq. Snellen: 20/100); C) Mes 6: LogMAR 0,7 (Eq. Snellen: 20/100).
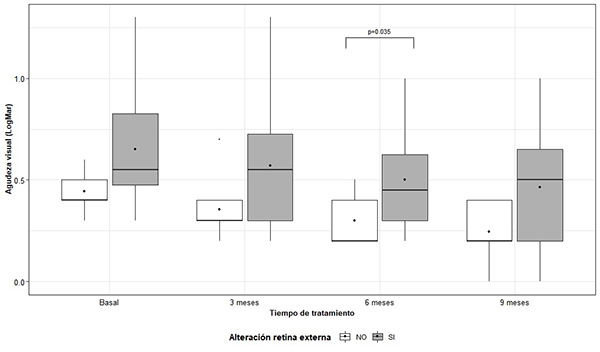
Figura 5: Distribución de AV (LogMar) de acuerdo al tiempo de medición y alteración de la retina externa.
Cantidad de puntos hiperreflectivos (PH)
La agudeza visual media, comparada según el número de PH, no mostró diferencias estadísticamente significativas en ninguno de los momentos de medición (Figura 6).
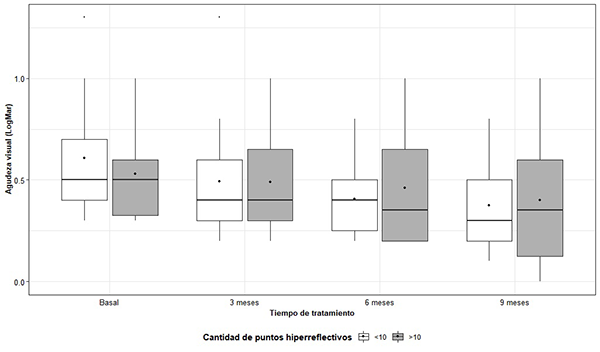
Figura 6: Distribución de AV (LogMar) de acuerdo al tiempo de medición y al número de puntos hiperreflectivos.
Al analizar el comportamiento de la agudeza visual, según escala LogMar, en forma longitudinal, se encontró que la misma presentó un decrecimiento estadísticamente significativo en función del tiempo de tratamiento (p < 0.001), sin diferir de acuerdo al número de puntos hiperrefectivos (efecto interacción: p=0.082) (Tabla 1).
Tabla 1: Resultado de los modelos univariados según el efecto de cada factor predictivo sobre la medición de AV en la línea de base y a través del tiempo.
Variable |
Efecto sobre la línea de base |
Efecto a través del tiempo |
AIC |
Estimado (EE) |
p |
Estimado (EE) |
p |
Tipo de edema macular (ref.: Cistoide) |
|
|
-43.452 |
Desprendimiento Seroso Subfoveal |
-0.215 (0.103) |
0.039 |
0.014 (0.008) |
0.079 |
Espongiforme |
0.034 (0.208) |
0.871 |
-0.009 (0.009) |
0.362 |
Traccional |
-0.427 (0.234) |
0.083 |
0.018 (0.010) |
0.094 |
DRIL (SÍ vs. No) |
0.188 (0.141) |
0.090 |
0.018 (0.007) |
0.009 |
-50.964 |
Alteración de la retina externa (Sí vs. No) |
0.166 (0.148) |
0.276 |
0.001 (0.007) |
0.913 |
-41.847 |
Cantidad de puntos hiperreflectivos
(>10 vs. <=10) |
-0.114 (0.158) |
0.477 |
0.012 (0.007) |
0.087 |
-43.614 |
Espesor macular central (Estandarizado) |
-0.066 (0.079) |
0.417 |
0.009 (0.003) |
0.007 |
-48.034 |
Espesor macular central (EMC)
La correlación entre la agudeza visual y el espesor macular central no resultó estadísticamente distinta de cero en ninguno de los tiempos de medición (Fig. 7). Sin embargo, se encontró que la modificación en la agudeza visual a lo largo del tiempo fue diferente en función del espesor macular central, siendo menor la disminución del valor LogMar a mayor espesor macular central (efecto interacción: p=0.005) (Tabla 1).
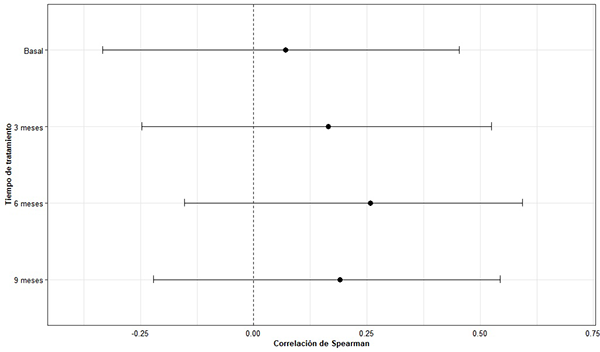
Figura 7: Distribución de AV (LogMar) de acuerdo al tiempo de medición y espesor macular central.
De acuerdo a los análisis longitudinales univariados. Según los valores de AIC, se obtiene un mejor ajuste de los datos cuando se considera la presencia o ausencia de DRIL como factor predictivo (Tabla 1).
Finalmente, se propuso un modelo longitudinal mixto considerando todos los biomarcadores en estudio, ajustados por el tipo de edema macular. En la Tabla 2 se muestran los resultados obtenidos tras el proceso de eliminación hacia atrás (backward). El tipo de edema macular, la presencia de DRIL y el espesor macular central fueron los factores que permanecieron en el modelo final, mostrando un efecto estadísticamente significativo sobre la modificación de la agudeza visual a lo largo del tiempo de tratamiento (efecto de las interacciones: p < 0.001 en todos los casos).
Tabla 2: Resultados del modelo multivariado que evalúa el efecto de cada factor predictivo en las mediciones de LogMar AV al inicio y a lo largo del tiempo (resultado de eliminación hacia atrás).
Variable |
Efecto en la línea de base |
Efecto sobre el cambio a lo largo del tiempo |
Estimado (EE) |
p |
Estimado (EE) |
p |
Tipo de edema macular (ref.: Cistoide) |
|
|
Desprendimiento seroso subfoveal |
-0.249 (0.089) |
0.006 |
0.018 (0.007) |
0.011 |
Espongiforme |
-0.135 (0.242) |
0.583 |
0.012 (0.009) |
0.200 |
Traccional |
0.540 (0.250) |
0.042 |
0.037 (0.009) |
< 0.001 |
DRIL (Sí vs. No) |
0.129 (0.150) |
0.402 |
0.024 (0.006) |
< 0.001 |
Espesor macular central (estandarizado) |
-0.108 (0.098) |
0.281 |
0.013 (0.003) |
< 0.001 |
EE= ERROR ESTÁNDAR
Para valores fijos de DRIL y espesor macular central, presentar desprendimiento seroso de la retina en lugar de edema macular cistoideo produce menor descenso en la medición de LogMar, al igual que sucede si se presenta compromiso traccional en lugar de edema macular cistoideo. El cambio en la agudeza visual no difiere entre los tipos de edema cistoide y espongiforme.
Para valores fijos de tipo de edema y espesor macular central, la presencia de DRIL se asocia a un menor descenso en la medición de LogMar. Finalmente, un mayor espesor macular central se relaciona con menor descenso en la medición de LogMar, considerando fijos el tipo de edema macular y la presencia de DRIL.
DISCUSIÓN
DRIL
Como es sabido, las capas plexiformes interna, nuclear interna y plexiforme externa de la retina contienen estructuras anatómicas críticas para la transmisión de datos visuales desde los fotorreceptores a las células ganglionares. La incapacidad de distinguir los límites entre estas capas, descrita recientemente como DRIL, sugiere probablemente una desorganización de algunos axones y núcleos de células amacrinas, bipolares y/u horizontales situados en estas zonas, y conduce a resultados visuales deficientes, como se puede observar en éste y otros estudios. También se ha planteado la hipótesis de que la desorganización se produce cuando los axones bipolares se rompen después de que se haya superado su límite elástico debido al edema.9, 2, 10, 11, 12
Este estudio demostró de forma consistente que, en el EMD existe una correlación entre la presencia de DRIL al inicio y la AV posterior aun tras la resolución del EMD. La AV final fue significativamente menor en comparación con los casos que no presentaban DRIL al inicio del tratamiento antiangiogénico. Los casos con presencia de DRIL mostraron un valor medio de LogMar a los 9 meses mayor que los que no tenían DRIL. También la modificación longitudinal de la AV fue significativa en función del tiempo y de la presencia de este biomarcador. Sun et al., describió la desorganización de las capas internas de la retina hallando una correlación negativa con la AV en ojos con EMD actual y, lo que es más importante, también en ojos en los que el EMD ya se ha resuelto; este fenómeno también se observó en nuestro estudio. También demostró que una mayor extensión del DRIL en la línea de base se correlaciona con una peor AV en la línea de base; en promedio, dentro de la zona foveal central de 1 mm, un aumento temprano de la DRIL de 300μm se asoció con un empeoramiento de la AV en 1 línea durante el período de seguimiento de 12 meses. 2
En 2015, Salma H. Radwan et al., también describió cuatro patrones de resolución del DRIL en pacientes con EMD, mostrando que la resolución temprana y tardía del DRIL mostraba una mayor reducción positiva del déficit de AV a los 8 meses, en comparación a los que no resolvieron, lo cuales mostraban una reducción negativa. Los mejores resultados de visión a los 8 meses se observaron en los ojos sin DRIL basal a lo largo de los 9 meses de tratamiento, incluso en los pacientes en los que el edema macular no se resolvió en su totalidad, en línea con nuestro estudio.10
Aunque en el presente trabajo las modificaciones en la extensión del DRIL a lo largo del tiempo no fueron consideradas, está claro que su presencia al inicio de la retinopatía es un predictor importante de pobre pronóstico visual más allá del tratamiento, y debería tenerse en cuenta a la hora de discutir las expectativas visuales con el paciente.
Tipos de edema macular diabético
Diversos estudios hasta la fecha han reportado diferentes categorías morfológicas de EMD basados en la OCT. Otani et al. reportó tres tipos morfológicos: esponjoso, cistoideo y desprendimiento seroso macular, mientras que Kim et al. consideró además la presencia de EMD de tipo traccional. Panozzo et al. por su lado identificó tres principales patrones morfológicos: un engrosamiento “simple” en el área macular, el subtipo cistoideo, y el de “desprendimiento neuroepitelial”, y clasificó la tracción epirretinal en cuatro tipos. 3, 4, 13
En contraste a lo reportado por los estudios realizados por Yamamoto y Otani, en los cuales el subtipo espongiforme fue el patrón hallado con mayor frecuencia (88% y 60% respectivamente, vs. 47% y 40% respectivamente para el tipo cistoideo), en el presente estudio el predominio fue del patrón cistoideo (48% vs. 20% espongiforme). Como sea, no debe considerarse clínicamente significativo como consecuencia de la pequeña población estudiada. 4, 14
El comportamiento longitudinal de la AV de acuerdo a la escala LogMAR mostró un decremento significativo en función del tiempo para todos los tipos de edema, sin notables diferencias entre ellos. En un estudio realizado por Kim et al., la AV media varió entre los diferentes subgrupos de EMD, aunque sólo de manera significativa para el de tipo cistoideo, que se asoció a peores resultados visuales. 3
Este estudio demostró que tanto el EMD asociado a un componente traccional de tipo vitreomacular, así como la presencia de edema seroso subfoveal (que es visible en el OCT como un área hiporreflectiva debajo de la neurroretina), tienen un efecto estadísticamente significativo sobre la modificación de la AV a lo largo de los 9 meses de tratamiento. En el componente traccional, la indicación de vitrectomía para liberar la tracción se hace imperiosa, mientras que el DSS ha tenido un rol controvertido como predictor de AV y cambios anatómicos finales y aún no quedan claros.
La prevalencia de DSS es de aproximadamente 15-30% en ojos con EMD, y se ha estudiado que tiene un importante componente inflamatorio, lo que lleva a considerar a los corticoesteroides intravítreos como una muy buena opción. 15
Un estudio en pacientes con EMD y DSS tratados con antiangiogénicos durante 12 meses, evidenció que no hubo diferencias en la AV en comparación con el grupo sin DSS, sin embargo, otros trabajos han mostrado que la presencia de este biomarcador se asocia con buena ganancia de AV y recuperación de la anatomía de la mácula. Los hallazgos del estudio RESTORE y el análisis post hoc del estudio RISE/RIDE mostraron un rol protector del SSD, evidenciando que la presencia del mismo en la línea de base se asoció con mejores resultados visuales al cabo de un año. 16, 17
Puntos hiperreflectivos (PH)
Los puntos hiperreflectivos son definidos como “lesiones discretas, bien circunscritas, con igual o mayor reflectividad que la banda del epitelio pigmentario de la retina”. 18
También descritos como manchas o focos hiperreflectivos, los PH se presentan en los ojos diabéticos incluso cuando la retinopatía es clínicamente indetectable; su número incrementa con el progreso de la retinopatía, y muestran una migración desde la retina interna a la retina externa. Una hipótesis bien aceptada, basada en algunos estudios histopatológicos, es la de la activación de células microgliales con la consecuente secreción de moléculas inflamatorias a nivel de la retina, asociado con muerte neuronal y endotelial. 15, 19
En el presente estudio, la AV media, comparada de acuerdo al número de PH, no mostró diferencias estadísticamente significativas en ninguno de los puntos de medición. Asimismo, se observó una reducción en el número de PH en la medida en que disminuyó el edema, siendo marcada en aquellos cuyo edema resolvió por completo. Esto se encuentra en línea con el estudio realizado por Carsten Framme et al., que evidenció buena respuesta al tratamiento antiangiogénico en términos anatómicos con desaparición de los PH, pero no necesariamente con buenos resultados visuales. 20 Sun et al. no encontró relaciones entre la presencia de PH y AV. 2
La naturaleza exacta de la relación entre PH y AV es todavía desconocida. Algunos estudios como aquellos llevados a cabo por Schreur et al. mostraron resultados contradictorios: mientras que en 2018 se vinculó la presencia de PH a malos resultados en AV (a pesar de no estar claro si el decremento en la AV fue secundario a la presencia de edema o no), en un estudio realizado en 2020 se demostró una potencial relevancia clínica de los PH como predictores de buena respuesta al tratamiento anti-VEGF o terapia corticoidea en EMD. Nuestro estudio no demostró una buena relación entre PH y AV, por lo que consideramos que deben ser tenidos en cuenta en combinación con biomarcadores de mayor fiabilidad para predecir la AV final. 7, 21
Alteraciones en las capas de la retina externa
Spaide et al. realizó una correlación de las bandas observadas en la retina externa por OCT, identificando cuatro: 1) Membrana Limitante Externa (MLE), 2) unión entre el segmento interno (SI) y externo (SE) de fotorreceptores (SE/SI), 3) membrana de Verhoeff (definida como una línea hiperrefringente por debajo de la SE/SI), y 4) EPR, posiblemente incluyendo a la membrana de Bruch y a la coriocapilaris. 22
En los estadíos recientes del EMD, la ruptura de la barrera hematorretiniana puede ocurrir, resultando en una acumulación de proteínas plasmáticas, lípidos, y fluido extracelular en la mácula. Este proceso podría estar relacionado con el daño a la MLE y SI/SE. La integridad de las capas de la retina externa es un indicador directo de salud de los fotorreceptores y el EPR. 22
Diversos estudios indican que una falta de integridad de las mismas en la OCT se relaciona a una peor AV post tratamiento, así como una mayor ganancia de AV final se ha encontrado en aquellos con un SI/SE indemnes. También un incremento en la visibilidad de la punta de segmento de los conos (también denominados en inglés cost: “cone outer segment tips”) a través del tiempo fue asociado con mejores AV. 2, 23, 24, 25
Con la ayuda del OCT, Shinichiro Ito et al. también describió una relación directamente proporcional entre la AV y el estado de la MLE, de los SE/SI, y de los segmentos externos de los conos, concluyendo en que debe ser usado como un biomarcador predictor de AV. 23
A pesar de esto, en nuestro estudio la AV mostró una mejoría estadísticamente significativa en función del tratamiento, sin diferir de acuerdo a la presencia o ausencia de alteraciones en la retina externa. Sin embargo, se halló una relación estadísticamente significativa al mes 6, en donde la ganancia de visión fue menor en el grupo con alteración de alguna de las capas externas (Fig. 1). Por su parte, Sun et al. tampoco encontró una relación consistente entre la AV y alteraciones reflectivas o cambios a nivel de la MLE o de la ZE, en contraste con los resultados que obtuvieron para el DRIL, en línea con nuestro estudio. 2
Por lo tanto, creemos que la integridad de las capas de la retina externa debe ser tomada en cuenta como una herramienta complementaria para el pronóstico de la visión del paciente al iniciar el tratamiento.
Espesor Macular Central (EMC)
El espesor retinal fue determinado como la distancia entre la superficie interna de la retina, definida como la interfase entre el vítreo oscuro y el reflejo brilloso de la membrana limitante interna, y la superficie de la retina externa. 27
La relación entre éste y la AV reducida es bien conocida y ha sido foco de atención y estudio en las últimas décadas, convirtiéndose en una herramienta clínica ciertamente útil. Asimismo otros biomarcadores le han ido ganando lugar a la par de la evolución de la tecnología OCT. Si bien se ha estudiado que un EMC aumentado se asociaría a un decremento en la AV, y que aquellos tratamientos que lo reducen mejorarían la visión, la evaluación cuantitativa de esta relación demostró ser controversial, y otros biomarcadores tienen en la actualidad más prominencia.
También se ha demostrado que la respuesta de la AV al tratamiento con láser focal al disminuir el grosor macular tras el tratamiento es paradójica hasta en un 26% de los ojos tratados, con una relación no más que moderada entre ambos, y afirmando que, aunque las mediciones del grosor retiniano con OCT representan un instrumento importante, no podrían reemplazar de manera confiable la AV frente a las distintas opciones terapéuticas. 28
ITO et al. demostró que pacientes con un EMC mayor a 250μm presentaron una correlación negativa con la AV, predisponiendo a una AV final más baja a pesar del tratamiento antiangiogénico. Pero también observaron que el espesamiento del EMC tal vez no tenga un efecto inmediato sobre la AV. De hecho, se observó que algunos pacientes mantuvieron una buena AV con un espesor macular aumentado y una capa de retina externa intacta en fases tempranas del EMD. Otani y asociados también demostraron que la AVMC está moderadamente correlacionada con el EMC, independientemente de las características tomográficas, sean pacientes con o sin EMD. 23, 28
En el presente estudio, el EMC también demostró una asociación significativa con los cambios en la AV. A lo largo del tratamiento, los que presentaron un aumento de EMC superior al promedio no lograron grandes mejoras en la AV en comparación con los que presentaron un EMC inicial inferior al promedio.
Debe considerarse al EMC una herramienta precisa e importante que puede ayudarnos a predecir una respuesta, aunque no sin asociar y considerar simultáneamente la presencia de otros biomarcadores que, en éste, y en estudios con mayor número de participantes, demostraron una asociación con la AV mayor a la del EMC.
CONCLUSIÓN
Es importante realizar una evaluación clínica detallada y un detenido análisis diagnóstico y pronóstico mediante la OCT, a través de la visualización de los diferentes biomarcadores estudiados hasta la actualidad.
El estudio demostró que al momento de proveer un pronóstico visual al paciente en contexto de iniciar un tratamiento antiangiogénico, es ciertamente útil evaluar el espesor macular central, aunque no de manera aislada; y, sobre todo, evaluar la presencia o ausencia de DRIL, que demostró ser el biomarcador tomográfico con mayor potencial para determinar una pobre ganancia de AV final a pesar del tratamiento antiangiogénico y resolución del EMC. Esto lo convierte en una excelente herramienta para, prospectivamente, determinar cuáles pacientes podrían tener una respuesta favorable o desfavorable, ayudaría a la selección terapéutica y reduciría el número de pacientes que se someten a tratamientos invasivos y prolongados e ineficaces.
Se necesitan más estudios que incorporen el análisis de los distintos biomarcadores en conjunto, incluyendo el de las nuevas tecnologías como el de la angiografía por OCT con biomarcadores tales como la densidad capilar, remodelamiento vascular, o el estudio de la zona avascular foveal, que, así como el DRIL, parecen prometedores como biomarcadores en el edema macular diabético.
Declaraciones
Aprobación de ética
Este estudio fue aprobado por el IRB del Instituto de Alta Complejidad Oftalmos, Buenos Aires, Argentina.
Consentimiento para publicación
No aplica
Disponibilidad de datos y materiales
Los conjuntos de datos utilizados y/o analizados durante el presente estudio están disponibles a petición del autor correspondiente
Conflictos de interés
CID, SP, ALC, LC, GD, PC y FDR declaran tener intereses contrapuestos.
AAA ha participado en consejos asesores de Roche, Alcon, Bayer y Novartis.
Financiación
No aplica
Autoría
CID Concepción del proyecto, diseño del estudio, adquisición de datos, redacción del artículo, aprobación de la versión final.
SP Redacción del artículo, revisión crítica intelectual, aprobación de la versión final.
ALC Análisis e interpretación de datos, redacción del estudio, y aprobación definitiva de la versión final.
LC Diseño del estudio, análisis estadístico e interpretación de los datos, aprobación definitiva de la versión final.
GD Diseño del estudio, revisión crítica del contenido intelectual, aprobación definitiva de la versión.
PC Análisis e interpretación de los datos, revisión crítica del contenido intelectual, aprobación definitiva de la versión final.
FDR Adquisición de imágenes de OCT, revisión crítica del contenido intelectual, aprobación definitiva de la versión final.
AAA Diseño del estudio, revisión crítica del contenido intelectual, aprobación definitiva de la versión final.
Todos los autores se comprometen a responder personalmente de sus propias contribuciones y a garantizar que las cuestiones relacionadas con la exactitud o la integridad de cualquier parte del trabajo, incluso aquellas en las que el autor no haya participado personalmente, se investiguen y resuelvan adecuadamente, y la resolución se documente en la bibliografía.
REFERENCIAS
1. Schmidt-Erfurth U, García-Arumi J, Bandello F, Berg K, Chakravarthy U, Gerendas BS, Jonas J, Larsen M, Tadayoni R, Loewenstein A. Guidelines for the Management of Diabetic Macular Edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica. 2017;237(4):185-222. doi: 10.1159/000458539. Epub 2017 Apr 20. PMID: 28423385.
2. Sun JK, Radwan SH, Soliman AZ, Lammer J, Lin MM, Prager SG, Silva PS, Aiello LB, Aiello LP. Neural Retinal Disorganization as a Robust Marker of Visual Acuity in Current and Resolved Diabetic Macular Edema. Diabetes. 2015 Jul;64(7):2560-70. doi: 10.2337/db14-0782. Epub 2015 Jan 29. PMID: 25633419; PMCID: PMC4477364.
3. Chung YR, Kim YH, Ha SJ, Byeon HE, Cho CH, Kim JH, Lee K. Role of Inflammation in Classification of Diabetic Macular Edema by Optical Coherence Tomography. J Diabetes Res. 2019 Dec 20;2019:8164250. doi: 10.1155/2019/8164250. PMID: 31930145; PMCID: PMC6939426.
4. Otani T, Kishi S, Maruyama Y. Patterns of diabetic macular edema with optical coherence tomography. Am J Ophthalmol. 1999 Jun;127(6):688-93. doi: 10.1016/s0002-9394(99)00033-1. PMID: 10372879.
5. Kaiser PK, Riemann CD, Sears JE, Lewis H. Macular traction detachment and diabetic macular edema associated with posterior hyaloidal traction. Am J Ophthalmol. 2001 Jan;131(1):44-9. doi: 10.1016/s0002-9394(00)00872-2. PMID: 11162978.
6. Phadikar P, Saxena S, Ruia S, Lai TY, Meyer CH, Eliott D. The potential of spectral domain optical coherence tomography imaging based retinal biomarkers. Int J Retina Vitreous. 2017 Jan 9;3:1. doi: 10.1186/s40942-016-0054-7. PMID: 28078103; PMCID: PMC5220620.
7. Schreur V, de Breuk A, Venhuizen FG, Sánchez CI, Tack CJ, Klevering BJ, de Jong EK, Hoyng Cb. Retinal Hyperreflective Foci in 1 diabetes mellitus. Retina. 2020 Aug;40(8):1565-1573. doi: 10.1097/IAE.0000000000002626. PMID: 31356496; PMCID: PMC7392582.
8. Markan A, Agarwal A, Arora A, Bazgain K, Rana V, Gupta V. Novel imaging biomarkers in diabetic retinopathy and diabetic macular edema. Ther Adv Ophthalmol. 2020 Sep 4;12:2515841420950513. doi: 10.1177/2515841420950513. PMID: 32954207; PMCID: PMC7475787.
9. Fickweiler W, Schauwvlieghe AME, Schlingemann RO, Maria Hooymans JM, Los LI, Verbraak FD; BRDME Research Group. Predictive value of optical coherence tomographic features in the bevacizumab and ranibizumab in patients with diabetic macular edema (BRDMe) study. Retina. 2018 Apr;38(4):812-819. doi: 10.1097/IAE.0000000000001626. PMID: 28406860.
10. Radwan SH, Soliman AZ, Tokarev J, Zhang L, van Kuijk FJ, Koozekanani DD. Association of Disorganization of Retinal Inner Layers with Vision After Resolution of Center-Involved Diabetic Macular Edema. JAMA Ophthalmol. 2015 Jul;133(7):820-5. doi: 10.1001/jamaophthalmol.2015.0972. PMID: 25950417.
11. Das R, Spence G, Hogg RE, Stevenson M, Chakravarthy U. Disorganization of Inner Retina and Outer Retinal Morphology in Diabetic Macular Edema. JAMA Ophthalmol. 2018 Feb 1;136(2):202-208. doi: 10.1001/jamaophthalmol.2017.6256. PMID: 29327033; PMCID: PMC5838716.
12. Pelosini L, Hull CC, Boyce JF, McHugh D, Stanford MR, Marshall J. Optical coherence tomography may be used to predict visual acuity in patients with macular edema. Invest Ophthalmol Vis Sci. 2011 Apr 25;52(5):2741-8. doi: 10.1167/iovs.09-4493. PMID: 20538987.
13. Panozzo G, Parolini B, Gusson E, Mercanti A, Pinackatt S, Bertoldo G, Pignatto S. Diabetic macular edema: an OCT-based classification. Semin Ophthalmol. 2004 Mar-Jun;19(1-2):13-20. doi: 10.1080/08820530490519934. PMID: 15658007.
14. Yamamoto T, Hitani K, Tsukahara I, Yamamoto S, Kawasaki R, Yamashita H, Takeuchi S. Early postoperative retinal thickness changes and complications after vitrectomy for diabetic macular edema. Am J Ophthalmol. 2003 Jan;135(1):14-9. doi: 10.1016/s0002-9394(02)01819-6. PMID: 12504691.
15. Vujosevic S, Bini S, Midena G, Berton M, Pilotto E, Midena E. Hyperreflective intraretinal spots in diabetics without and with nonproliferative diabetic retinopathy: an in vivo study using spectral domain OCT. J Diabetes Res. 2013;2013:491835. doi: 10.1155/2013/491835. Epub 2013 Dec 9. PMID: 24386645; PMCID: PMC3872101.
16. Giocanti-Aurégan A, Hrarat L, Qu LM, Sarda V, Boubaya M, Levy V, Chaine G, Fajnkuchen F. Functional and Anatomical Outcomes in Patients With Serous Retinal Detachment in Diabetic Macular Edema Treated With Ranibizumab. Invest Ophthalmol Vis Sci. 2017 Feb 1;58(2):797-800. doi: 10.1167/iovs.16-20855. PMID: 28152140.
17. Reddy RK, Pieramici DJ, Gune S, Ghanekar A, Lu N, Quezada-Ruiz C, Baumal CR. Efficacy of Ranibizumab in Eyes with Diabetic Macular Edema and Macular Nonperfusion in RIDE and RISE. Ophthalmology. 2018 Oct;125(10):1568-1574. doi: 10.1016/j.ophtha.2018.04.002. Epub 2018 May 8. PMID: 29752001.
18. Ho J, Witkin AJ, Liu J, Chen Y, Fujimoto JG, Schuman JS, Duker JS. Documentation of intraretinal retinal pigment epithelium migration via high-speed ultrahigh-resolution optical coherence tomography. Ophthalmology. 2011 Apr;118(4):687-93. doi: 10.1016/j.ophtha.2010.08.010. Epub 2010 Nov 20. PMID: 21093923; PMCID: PMC3070873.
19. Joussen AM, Doehmen S, Le ML, Koizumi K, Radetzky S, Krohne TU, Poulaki V, Semkova I, Kociok N. TNF-alpha mediated apoptosis plays an important role in the development of early diabetic retinopathy and long-term histopathological alterations. Mol Vis. 2009 Jul 25;15:1418-28. PMID: 19641635; PMCID: PMC2716944.
20. Framme C, Schweizer P, Imesch M, Wolf S, Wolf-Schnurrbusch U. Behavior of SD-OCT-detected hyperreflective foci in the retina of anti-VEGF-treated patients with diabetic macular edema. Invest Ophthalmol Vis Sci. 2012 Aug 24;53(9):5814-8. doi: 10.1167/iovs.12-9950. PMID: 22836760.
21. Schreur V, Altay L, van Asten F, Groenewoud JMM, Fauser S, Klevering BJ, Hoyng CB, de Jong EK. Hyperreflective foci on optical coherence tomography associate with treatment outcome for anti-VEGF in patients with diabetic macular edema. PLoS One. 2018 Oct 31;13(10):e0206482. doi: 10.1371/journal.pone.0206482. PMID: 30379920; PMCID: PMC6209345.
22. Spaide RF, Curcio CA. Anatomical correlates to the bands seen in the outer retina by optical coherence tomography: literature review and model. Retina. 2011 Sep;31(8):1609-19. doi: 10.1097/IAE.0b013e3182247535. PMID: 21844839; PMCID: PMC3619110.
23. Ito S, Miyamoto N, Ishida K, Kurimoto Y. Association between external limiting membrane status and visual acuity in diabetic macular oedema. Br J Ophthalmol. 2013 Feb;97(2):228-32. doi: 10.1136/bjophthalmol-2011-301418. Epub 2012 Nov 21. PMID: 23172879.
24. Forooghian F, Stetson PF, Meyer SA, Chew EY, Wong WT, Cukras C, Meyerle CB, Ferris FL 3rd. Relationship between photoreceptor outer segment length and visual acuity in diabetic macular edema. Retina. 2010 Jan;30(1):63-70. doi: 10.1097/IAE.0b013e3181bd2c5a. PMID: 19952996; PMCID: PMC3021331.
25. Maheshwary AS, Oster SF, Yuson RM, Cheng L, Mojana F, Freeman WR. The association between percent disruption of the photoreceptor inner segment-outer segment junction and visual acuity in diabetic macular edema. Am J Ophthalmol. 2010 Jul;150(1):63-67.e1. doi: 10.1016/j.ajo.2010.01.039. Epub 2010 May 10. PMID: 20451897; PMCID: PMC2900476.
26. Murakami T, Nishijima K, Sakamoto A, Ota M, Horii T, Yoshimura N. Association of pathomorphology, photoreceptor status, and retinal thickness with visual acuity in diabetic retinopathy. Am J Ophthalmol. 2011 Feb;151(2):310-7. doi: 10.1016/j.ajo.2010.08.022. Epub 2010 Dec 9. PMID: 21145531.
27. Kim BY, Smith SD, Kaiser PK. Optical coherence tomographic patterns of diabetic macular edema. Am J Ophthalmol. 2006 Sep;142(3):405-12. doi: 10.1016/j.ajo.2006.04.023. PMID: 16935584.
28. Diabetic Retinopathy Clinical Research Network, Browning DJ, Glassman AR, Aiello LP, Beck RW, Brown DM, Fong DS, Bressler NM, Danis RP, Kinyoun JL, Nguyen QD, Bhavsar AR, Gottlieb J, Pieramici DJ, Rauser ME, Apte RS, Lim JI, Miskala PH. Relationship between optical coherence tomography-measured central retinal thickness and visual acuity in diabetic macular edema. Ophthalmology. 2007 Mar;114(3):525-36. doi: 10.1016/j.ophtha.2006.06.052. Epub 2006 Nov 21. PMID: 17123615; PMCID: PMC2585542.