ARCH ARGENT OFTALMOL | 2018
ARTÍCULO DE INTERÉS
Tecnologías
para la emetropía
Relator:
Dr. Julio Fernández Mendy
Co-Relatores:
Dr. Omar López Mato, Dra. María José Cosentino, Dr. Roger Zaldivar, Dr. Roberto Albertazzi,
Dr. Roberto Zaldivar, Dr. Daniel Badoza, Dr. Carlos Ferroni
El Relato Anual de la Sociedad Argentina de Oftalmología, constituye una tradición desde hace muchas décadas, inspirado en el Rapport Annuelle de la Société Française d’Ophtalmologie.
La elección del Relato Anual SAO 2017 “Tecnologías para la Emetropía” fue realizada durante el Congreso Argentino de Oftalmología 2015.
Recuerdo aquí que se elige durante un día completo del Congreso Anual de la SAO y se pueden presentar los miembros titulares de la Sociedad, proponiendo el título del Relato Anual que, en caso de ganar, será leído dos años más tarde, en el futuro congreso.
El relator elige los co-relatores, que van a colaborar en la presentación del Relato Anual durante la sesión del Congreso Anual que les corresponda.
INTRODUCCIÓN
Desde muy temprano en la historia de la humanidad, se han desarrollado diferentes instrumentos, algunos muy primitivos, otros más elaborados, desde unos extremadamente simples, hasta los actuales muy sofisticados, para combatir los vicios de refracción e intentar alcanzar finalmente la emetropía.
Obtener la emetropía absoluta, de manera completa, sin aberraciones de ningún tipo, quizás sea una utopía, no obstante, el avance obtenido en los últimos 50 años nos alienta en el camino hacia la meta anhelada.
El presente relato tiene la intención de mostrar los grandes logros alcanzados hasta ahora y los desafíos que todavía quedan por resolver.
Para este fin contamos con la participación de prestigiosos colegas, conocedores profundos de cada tema, a quienes agradezco especialmente la presentación que hicieron en el Congreso Conjunto de Oftalmología 2017 en el que se presentó este Relato Anual.
HISTORIA
Tecnologías desde la antigüedad hasta la Segunda Guerra Mundial
En el siglo II antes de Cristo, la percepción de los objetos y la naturaleza de este fenómeno generó una discusión en la Grecia Antigua entre Demócrito, quien concebía el proceso de la visión como un fenómeno puramente físico-material, y Aristóteles que le adicionaba un componente de percepción psíquica.
Aristóteles, sostenía que el intelecto y el alma eran estables en el tiempo, que no envejecían, y consideraba que el deterioro de la visión con la edad (la presbicia) se debía a un deterioro del órgano y que “si un anciano pudiera disponer de un ojo apropiado vería, sin duda, igual que un joven” (Acerca del alma I 4, 408b 22) y explica que la pérdida de la agudeza se debía a que, al igual que la piel se arruga con el paso del tiempo, por pérdida de humedad, la piel que recubre la pupila también se arruga perdiendo la transparencia.
En el siglo II después de Cristo fue Ptolomeo, quien, tomando las ideas de Aristóteles, comienza analizando las ametropías como consecuencia de la morfología de los ojos: “Aquellos que tienen ojos profundos ven más lejos que aquellos que no tienen tales ojos; y la razón de esto es que la potencia visual de aquellos está comprimida, ya que, al emanar a través de sitios estrechos, el flujo visual se comprime y alarga”
En la Edad Media, los escritos de los griegos clásicos son tomados por árabes y cristianos que lo difunden por toda la Europa Mediterránea.
Johannes Kepler en 1611 reconoce el origen aristotélico de los términos miopía y presbicia, y es el primero en dar una explicación a la miopía e hipermetropía, por lo cual su influencia en la ciencia óptica moderna es capital.
Aunque desde el siglo XII antes de Cristo existen, en Mesopotamia (Asiria), Egipto, India o Grecia (Creta), piedras de cristal, que algunos suponen como los primeros anteojos, se cree que eran elementos para encender el fuego.
Algunas piedras magnificadoras (plano-convexas), quizás fueron inventadas para lectura, fabricadas de vidrio, a partir de la arena de cuarzo y berilio.
La Óptica, como disciplina, se debe al médico árabe Alhazen (965-1039 dc) quien sostiene que la visión es posible por los rayos de luz que entran al ojo y no porque de los ojos emanen rayos de luz (como sostenía la medicina de la época). Escribió un tratado que llamó Óptica donde comienza a desarrollar el estudio de las leyes que rigen la física óptica.
Los primeros lentes dobles para ser colocados sobre la nariz (anteojos o gafas), se estima que aparecieron en el siglo XIII. No existe la certeza de dónde provienen, pero se cree que se originaron en China y algunas fuentes dicen que fue Marco Polo quien los introduce en Venecia.
Unas versiones sostienen que fue Roger Bacon, un monje franciscano, el inventor de los anteojos, otras, aseguran que fue en Florencia, y fueron Alessandro della Spina y Salvino degli Armatti los inventores. Originalmente consistían en dos círculos de madera o asta unidos por un remache.
El Renacimiento fue un momento de la Humanidad en el cual la creatividad alcanzó uno de sus puntos más elevado. La revolución en las artes fue acompañada por cambios paradigmáticos en las ciencias. La experimentación dio lugar a un progreso de la tecnología en muchas ramas y la óptica no fue ajena a estos cambios.
Leonardo da Vinci fue uno de los más sorprendentes innovadores. Descubrió el principio de la cámara oscura con un orificio estenopeico que permitía proyectar la imagen invertida en una pantalla, de donde se valía para realizar los croquis de sus obras. Entre muchos de los inventos esbozó la idea de lo que serían, muchos siglos después, los lentes de contacto.
Entre los instrumentos ópticos desarrollados en esa época, sin duda los más importantes fueron el telescopio (Galileo Galilei) y el microscopio (Leeuwenhoek) que serían revolucionarios para algunas ciencias: la Astronomía, la Botánica, la Biología, la Medicina, etc. permitiendo el desarrollo ulterior de muchas de las novedades que surgieron, ya en el siglo XIX, en cuanto a nuestra búsqueda de la emetropía.
La evolución hacia la obtención de la corrección de los vicios de refracción necesitó, imperiosamente, la evolución en la tecnología del diagnóstico de esos defectos refractivos y la tecnología de los elementos que se utilizaron para corregirlos. Cada paso en la progresión de la aparatología en el diagnóstico generó una nueva posibilidad de progresión en la técnica quirúrgica para corregirla.

Anteojos medievales

El primer microscopio de Leeuwenhoek.
CIRUGÍAS INICIALES PARA CORREGIR LOS VICIOS DE REFRACCIÓN
Hacia 1850 Albretch Von Graefe comenzó a realizar la cirugía de catarata ab externo extrayendo el cristalino con una incisión limbar. Una de las consecuencias fue descubrir que este tipo de incisión inducía astigmatismo. Esta observación llevó hacia 1880 a realizar incisiones relajantes para corregir astigmatismos. Es el comienzo de la Cirugía Corneal Incisional.
En esta etapa hubo un aprendizaje sobre el camino, ya que el procedimiento era muy empírico y poco sistematizado. Obviamente este avance fue permitido por el desarrollo de un instrumento muy importante que hoy se conoce como queratómetro de Javal, que permitía realizar la medición de la cara anterior de la córnea.
Emile Javal, en 1880 presentó en el Congreso Internacional de Milán, el Ophtalmometre.
Existen controversias en cuanto a que, quien lo inventó fue el médico y físico alemán Hermann von Helmholtz, pero quien quedó ligado a este instrumento, por más de un siglo, fue el francés Javal quien sólo hizo una modificación convirtiéndolo en un instrumento muy fácil de utilizar. También al noruego Schiotz, quien fue más reconocido mundialmente por el tonómetro, se lo asocia frecuentemente en el oftalmómetro.
El oftalmómetro (debería decirse queratómetro) de Javal-Schiotz tuvo vigencia por más de 100 años cuando fue superado por los autorrefractómetros automatizados y más recientemente por los topógrafos. El principio, que era simple pero muy preciso en medir la curvatura de la cara anterior de la córnea, continuó siendo el mismo en los queratómetros actuales.
El primero en analizar cuantitativamente el efecto de las incisiones corneales fue un holandés, Leendert Jans Lans, en 1898, al publicar un “Experimental studies of the treatment of astigmatism with non-perforating corneal incisions”. En este estudio realizado en conejos analizaba los efectos de cada tipo de incisión sobre la córnea. Sus resultados ya anticipan algunas reglas, ciertas leyes básicas que posteriormente se aplicarán en la queratotomía.
El pionero de la Cirugía Refractiva Corneal Incisional fue Tsutomu Sato, en Japón, quien realizó varios procedimientos de queratotomía radial para tratar la miopía entre 1930 y 1950. El procedimiento consistía en realizar numerosas incisiones radiales en la cara anterior (40) y también en la cara posterior corneal (45) con las que aplanaba la córnea central. Sato publicó en 1939 en Acta Soc Ophthalm Jap “Treatment of conical incisión of Descemet’s Membrane” que proponía para corregir en queratocono y astigmatismo, y en 1953 en el American Journal of Ophthalmology un artículo titulado “A new surgical approach to myopia” donde vierte su experiencia en 32 casos de miopía, bajo anestesia retrobulbar y previa miosis. Los trabajos de Sato no proporcionaron resultados muy alentadores. Su procedimiento no aportaba gran corrección óptica, no era previsible y las complicaciones de la cirugía eran inaceptables, pues el 75% de los pacientes desarrollaron queratopatía bullosa. Curiosamente, en esa época, no se conocían bien las funciones del endotelio corneal y Sato hacía 45 incisiones radiales en el endotelio y la membrana de Descemet. Afortunadamente detuvo sus trabajos, ante la inexactitud del procedimiento y la aparición de los lentes de contacto, y no por las descompensaciones corneales que sobrevinieron luego de su temprana muerte.
La otra vertiente para corregir vicios de refracción fue la Cirugía con Extracción del Cristalino. En 1889 el oftalmólogo polaco, Vincent Fukala ante la Sociedad Médica de Viena, presenta su técnica de extracción del cristalino en los casos de miopía progresiva. Describió sus primeros 2 casos, y luego realizó en los años siguientes otros 19 casos, con buenos resultados refractivos según lo refirió.
La idea no fue suya. En 1776 Abbé Desmonceaux, se cree fue el primero en realizar tal cirugía, en Francia, no obstante, la extracción del cristalino para corregir la miopia fue bautizada como procedimiento de Fukala.
A pesar de su entusiasmo, las discusiones en esa época fueron muy importantes. Se lo criticaba porque en principio no detenía la miopía, pero sobre todo la controversia se desarrolló sobre el desprendimiento de retina. Algunos sostenían que la intervención lo evitaba, otros que no lo evitaba y otros que lo favorecían. En algunas discusiones académicas refieren las crónicas que se llegó a plantear que era criminal hacer esta operación.
La pérdida de vítreo, el glaucoma la infección eran las complicaciones que ocurrían, y muchos pacientes dados por curados, inicialmente, después tuvieron en muchos casos una pérdida visual severa.
En 1903 Muller fue el primero en realizar otra técnica que intentaba corregir la miopía con resecciones esclerales, con el objetivo de acortar el globo ocular. Dentro del mismo concepto Jorge Malbrán y José Ignacio Barraquer propusieron el “cinchamiento” del globo con una banda de fascia Iata o de esclera, aplicada a manera de cinturón, disminuyendo antero-posteriormente el globo, reforzando la esclera en la región de la mácula. Esta intervención, obtuvo algunos buenos resultados inmediatos, pero era un procedimiento muy traumático.
Así llegamos al fin de la Segunda Guerra Mundial, cuando surge la genial idea de Harold Ridley de crear un lente intraocular, que va a revolucionar nuestra especialidad y provocar cambios vertiginosos.
LENTE INTRAOCULAR CON EXTRACCIÓN DE CRISTALINO
La era de los lentes intraoculares que reemplazan al cristalino con catarata, comienza con el primer implante de Sir Harold Ridley, que ocurrió el 29 de noviembre de 1949 en el St. Thomas and Moorfields de Londres.

Sir Harold Ridley
Sus dos primeros casos fueron malos en la predicción del cálculo, ya que quedaron en -18 -6 a 120 º y -10 -2 a 60º respectivamente, debido a que el implante original fue calculado en el aire, era más grande y más grueso que lo debido. Los siguientes implantes obtuvieron resultados muy aceptables en las predicciones, considerando la tecnología de esa época. Realizó un caso en 1949, 3 casos en 1950 y 23 en 19511.
El primer implante era un lente monopieza de 8.35 mm de diámetro, 2.4 mm de espesor y superficies anterior y posterior diferentes (10 mm y 6 mm de radios de curvatura), fabricado en un material llamado Perspex (o Plexiglass) luego conocido como PoliMetilMetAcrilato (PMMA).
El índice refractivo era de 1.49 y el poder en el aire de +74D y en un medio como el acuoso, con un índice de refracción de 1.33, para un lente de +24D en el humor acuoso1.
Lo que pretendía conseguir Ridley con su innovación no era la emetropía, sino evitar un problema que generaba la afaquia en esa época, que era la pérdida de la visión binocular en las cataratas monoculares y que no podían corregirse con lentes de contacto debido a intolerancia1.
A partir de los comienzos de Ridley, en las décadas del 50 y 60, la cirugía del cristalino se había inclinado hacia la extracción intracapsular.
Aunque Jacques Daviel había sido el pionero, en 1750, en realizar la cirugía extracapsular, esta técnica había caído en desuso, sobre todo luego de la invención del crio, a partir de una idea del polaco Krawicz en 1961 y el desarrollo de Charles Kelman en conjunto con un neurocirujano americano Irving Cooper18 quienes en 1963 inventaron el crioestractor que llamaron cryostilet.
Por ese motivo, el diseño de los siguientes lentes intraoculares que continuaron al de Ridley fue el de los diseñados, principalmente, para ser insertados en cámara anterior, con soporte angular o fijados en el iris.
Luego de años y numerosas complicaciones corneales con los primeros lentes intraoculares de cámara anterior, se regresa a la cirugía extracapsular y se comienza con el diseño de los lentes de cámara posterior de Charles Kelman que siguen siendo, con pequeñas variantes, el de los actuales.
Aquí también, la tecnología condicionó la técnica quirúrgica, pensemos que hasta los 70 se operaba con lupas y que, es a partir de allí, cuando se comenzó a utilizar el microscopio quirúrgico para realizar la cirugía de catarata.

Charles Kelman
En esos años, 1967, comienza el desarrollo de una tecnología que va a permitir la era de la cirugía facorrefractiva veinte años después: la facoemulsificación, otra creación brillante de Kelman, que ideó un procedimiento pensando extraer la catarata a través de una incisión pequeña, con el objeto de evitar el astigmatismo, con la mínima invasión. Tengamos en cuenta que se estaba operando con una incisión de 10 a 12 mm con técnica intracapsular o extracapsular. Kelman también consideraba una ventaja importante, la máxima rapidez en la recuperación post quirúrgica.
La idea genial surge casi por casualidad, en febrero de 1963, sentado en un sillón del odontólogo, cuando observó el instrumental con el que le realizaban obturaciones dentales y pensó que un instrumento delgado podía ser introducido dentro del ojo a través de una incisión pequeña, desmenuzar, fragmentar o pulverizar el material nuclear y retirarla a través de una pequeña incisión40.
El primer facoemulsificador fabricado por Kelman comenzó a ser utilizado en 1967, cuando realiza su primer reporte, describe la técnica y los resultados en cirugías realizadas a ojos de cadáveres y de animales in vivo. Recién en 1974 aparecen sus publicaciones sobre experiencias con facoemulsificación en ojos humanos41-42.
CIRUGÍAS INICIALES CORNEALES POR SUSTRACCIÓN
José Ignacio Barraquer (1916-98), hijo de un prestigioso oftalmólogo catalán, quien se trasladó a Bogotá en 1953, fundó el Instituto Barraquer de América en 1964 y la Clínica Barraquer en 1968. Fue quien introdujo la idea del tratamiento con sustracción y adición en la córnea. En 1958 publicó un trabajo “Método para la talla de injertos laminares en córnea congelada; nueva orientación para la cirugía refractiva”21.
En 1964 publicó “Queratomileusis para la corrección de la miopía” y, en el prefacio, explica el significado de la palabra keratomileusis, término proveniente del griego, cuyo significado es el de tallado de la córnea. En esa publicación, describe un instrumento creado por él mismo, el microquerátomo 22.
En 1965 publica otro trabajo, en homenaje a su padre, en el que expone las “Bases de la queratoplastia refractiva” en el cual sienta las bases de la “Ley de los espesores” 23 y anticipa lo que piensa de la cirugía refractiva:
“La cirugía de la refracción es una nueva rama de la cirugía ocular, destinada a alcanzar un gran desarrollo en el transcurso de los próximos años. Si bien su meta es la supresión de todo defecto de refracción significativo, en la actualidad, su campo de acción está restringido a prevenir la creación de ametropías, consecuencia de procesos patológicos o quirúrgicos, a corregir aquellas en las que las prótesis habituales no permiten obtener un resultado satisfactorio. Deben mencionarse aquí, aunque sea brevemente, las intervenciones de Ridley, Strampelli y derivadas, tendientes a modificar el sistema óptico del ojo por medio de la inclusión de un lente intraocular, actualmente en desuso, dado el alto porcentaje de complicaciones tardías”.
Es muy interesante analizar esta frase del Gran José Ignacio Barraquer, uno de los oftalmólogos más brillantes, que forma parte del ASCRS Ophthalmology Hall of Fame como Innovator de la década del ’60, porque estaba en lo cierto sobre que la cirugía sobre el espesor corneal, sobre la que venia trabajando le veía un futuro promisorio en los años siguientes, no así la de los lentes intraoculares que atravesaban su peor momento. Allí hizo falta un cambio, y otro genio como él, que fue Kelman, con el desarrollo del Facoemulsificador y con los lentes intraoculares de cámara posterior.
A partir de estas premisas Barraquer realizó la queratomileusis, cortando un lentículo corneal con el microquerátomo, luego congelándolo y tallando con el criotorno, por la cara estromal, el defecto refractivo a corregir.
Esta cirugía es la queratomileusis por congelación, que fue el primer procedimento por sustraccion tisular para corregir las ametropías.

Máquina de facoemulsificación de Kelman

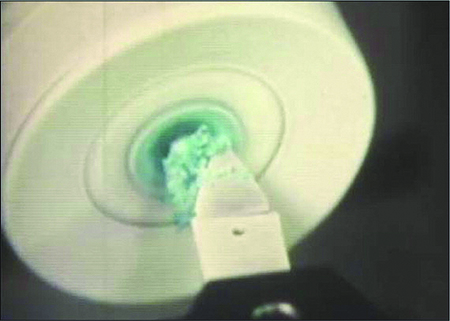
Microquerátomo y Criotorno diseñado por Barraquer

José Ignacio Barraquer
CIRUGÍA SOBRE EL CRISTALINO CON LENTES INTRAOCULARES
La década de 1980 fue la del auge de la cirugía extracapsular (ECCE), con todas sus variantes.
La aparición de los viscoelásticos en esa época cambió la precisión de las maniobras en cámara anterior, aunque la cirugía extracapsular se realizaba sin viscoelástico, con quistítomo y mantenedor de cámara y la colocación del lente bajo aire, con lo cual el lente era imposible implantarlo en el bag.
La técnica habitual de ECCE consistía en: incisión esclero-corneal de 10 mm, uso de viscoelástico, capsulotomía en abrelata, expresión del núcleo con maniobra bimanual, cierre parcial de la herida y aspiración de masas con cánula de irrigación/aspiración, o con bomba de irrigación/aspiración y luego con viscoelástico o bajo aire, colocación del LIO donde quede.
La endosacular o intercapsular, creada en Bélgica por Albert Galand y Camile Budo, fue otra técnica en la que se realizaba incisión corneal superior, capsulotomía lineal de hora 2 a 10 con aguja, luego de extraer el núcleo con maniobra de expresión bimanual y aspirar la corteza con técnica manual (cánula de doble vía), se colocaba el lente bajo viscoelástico dentro del bag, terminando con una capsulorrexis inferior en forma de letra D hacia abajo. Esta técnica fue la primera en garantizar la colocación del lente dentro del saco.
Otra técnica de esta década fue el Mini Nuc, que fue una técnica difundida por Michael Blumenthal, de Israel, en donde se extrae el núcleo a través de una incisión de 5 mm escleral con un túnel largo con una expansión lateral de la entrada corneal en cámara, creando una especie de embudo, que permite extraerlo con la hidropresión de un mantenedor de cámara colocado inferior y haciendo contrapresión en la entrada escleral.
En esta época los lentes de cámara posterior más utilizados son los de hápticas de prolene en J o en C, modelo Kelman con óptica de PMMA de 6 ó 7 mm de diámetro. Algunos detalles diferencian estos modelos: en algunos se crean agujeros en la óptica para posicionar el lente con ganchos de Sinsky o el primer invento de quien luego será famoso, Robert Osher, quien creó el háptica con un rulo final que permite manipularla con un gancho al que se denominaba “el Osher”.
Otros modelos de LIOs de los ’80 son los de forma de plato, redondos sin hápticas, como los diseñados por Albert Galand, de 9 mm de diámetro de PMMA o el de Azis Annis, con óptica de PMMA, de 6 ó 7 mm con hápticas circulares de prolene que cubren cada una de ellas 180°.
En 1984 Mazzocco implantó el primer lente plegable de silicona, que en 1995 era el material preferido por los oftalmólogos con el 37% y recién disminuye hacia 2003 al 13% en las encuestas realizadas en el ASCRS61.
El lente plegable fue la consecuencia del trabajo que Charles Kelman había estado dedicando incansablemente durante décadas, creyendo en su invento, mejorando su tecnología y pensando que el futuro era la incisión pequeña y el ultrasonido. Pero era necesario tener un lente que fuera viable para hacer cambiar a los cirujanos a esta nueva técnica, cuya transición era compleja, pero el resultado valía la pena ese esfuerzo.
La década de 1990 es la década en la cual la facoemulsificación supera a la extracapsular y finalmente se impone realizar una cirugía de extracción del cristalino a través de una pequeña incisión y colocando un lente intraocular en el saco capsular con total seguridad.

Primer lente plegable de silicon
A esto contribuyeron los conocimientos que anteriormente estuvimos analizando en cuanto a la cirugía incisional corneal, la inducción del astigmatismo y de innovaciones de la técnica quirúrgica, que fueron verdaderos paradigmas para lograr la emetropía, como la capsulotomía circular continua (CCC) que fueron descriptas por Howard Gimbel y Tomas Neuhamm. La aparición de la técnica depurada de esta maniobra, que hoy aprende un residente al comenzar sus primeras cirugías ocurrió muchos años después del concepto de la cirugía extracapsular con lente intraocular.
A esto contribuyeron los conocimientos que anteriormente estuvimos analizando en cuanto a la cirugía incisional corneal, la inducción del astigmatismo y de innovaciones de la técnica quirúrgica, que fueron verdaderos paradigmas para lograr la emetropía, como la capsulotomía circular continua (CCC) que fueron descriptas por Howard Gimbel y Tomas Neuhamm. La aparición de la técnica depurada de esta maniobra, que hoy aprende un residente al comenzar sus primeras cirugías ocurrió muchos años después del concepto de la cirugía extracapsular con lente intraocular.
Antes que esta maniobra fuera descripta, el LIO podía colocarse en el saco o en el surco y el cirujano no podía asegurarse que así fuera, esta diferencia en el posicionamiento del lente provoca una diferencia en la refracción que puede llegar a ser de 1 D en los poderes altos y 0.50 D en los medios.
Remarco la importancia que para mí tiene la CCC en alcanzar la emetropía, pues el porcentaje de lentes en el bag que ocurría con certeza con la capsulotomía en abrelatas era muy bajo.
Una vez logrado este nivel de perfección en la técnica depurada de la catarata, con una incisión pequeña que induce poco astigmatismo, garantizada la colocación de un lente perfectamente ubicado en el bag, con un overlapping de la capsula anterior en 360°, recién es posible obtener una mejora en el cálculo del LIO ya que la posición del lente en el bag reduce una importantísima fuente de error.
| Power at Capsular Bag |
Power at |
|
|
| Cilliary |
|
|
|
| Sulcus |
Bag / Sulcus Difference |
Subtract from Bag Power |
| +30.00 D |
+28.55 D |
-1.45 D |
-1.50 D |
| +29.50 D |
+28.09 D |
-1.42 D |
-1.50 D |
| +29.00 D |
+27.61 D |
-1.39 D |
-1.50 D |
| +28.50 D |
+27.14 D |
-1.36 D |
-1.50 D |
| +28.00 D |
+26.67 D |
-1.33 D |
-1.00 D |
| +27.50 D |
+26.20 D |
-1.30 D |
-1.00 D |
| +27.00 D |
+25.73 D |
-1.27 D |
-1.00 D |
| +26.50 D |
+25.26 D |
-1.25 D |
-1.00 D |
| +26.00 D |
+24.79 D |
-1.22 D |
-1.00 D |
| +25.50 D |
+24.31 D |
-1.19 D |
-1.00 D |
| +25.00 D |
+23.84 D |
-1.16 D |
-1.00 D |
| +24.50 D |
+23.36 D |
-1.13 D |
-1.00 D |
| +24.00 D |
+22.89 D |
-1.11 D |
-1.00 D |
| +23.50 D |
+22.42 D |
-1.08 D |
-1.00 D |
| +23.00 D |
+21.94 D |
-1.05 D |
-1.00 D |
| +22.50 D |
+21.47 D |
-1.03 D |
-1.00 D |
| +22.00 D |
+21.00 D |
-1.00 D |
-1.00 D |
| +21.50 D |
+20.53 D |
-0.97 D |
-1.00 D |
| +21.00 D |
+20.05 D |
-0.95 D |
-1.00 D |
| +20.50 D |
+19.58 D |
-0.92 D |
-1.00 D |
| +20.00 D |
+19.11 D |
-0.89 D |
-1.00 D |
| +19.50 D |
+18.63 D |
-0.87 D |
-1.00 D |
| +19.00 D |
+18.16 D |
-0.84 D |
-1.00 D |
| +18.50 D |
+17.69 D |
-0.82 D |
-1.00 D |
| +18.00 D |
+17.21 D |
-0.79 D |
-1.00 D |
| +17.50 D |
+16.73 D |
-0.77 D |
-1.00 D |
| +17.00 D |
+16.26 D |
-0.74 D |
-0.50 D |
| +16.50 D |
+15.78 D |
-0.72 D |
-0.50 D |
| +16.00 D |
+15.31 D |
-0.69 D |
-0.50 D |
| +15.50 D |
+14.83 D |
-0.67 D |
-0.50 D |
| +15.00 D |
+14.35 D |
-0.64 D |
-0.50 D |
| +14.50 D |
+13.88 D |
-0.62 D |
-0.50 D |
| +14.00 D |
+13.40 D |
-0.60 D |
-0.50 D |
| +13.50 D |
+12.93 D |
-0.57 D |
-0.50 D |
| +13.00 D |
+12.45 D |
-0.55 D |
-0.50 D |
| +12.50 D |
+11.97 D |
-0.53 D |
-0.50 D |
| +12.00 D |
+11.49 D |
-0.50 D |
-0.50 D |
| +11.50 D |
+11.02 D |
-0.48 D |
-0.50 D |
| +11.00 D |
+10.54 D |
-0.46 D |
-0.50 D |
| +10.50 D |
+10.07 D |
-0.43 D |
-0.50 D |
| +10.00 D |
+9.58 D |
-0.41 D |
-0.50 D |
| +9.50 D |
+9.11 D |
-0.39 D |
-0.50 D |
| +9.00 D |
+8.63 D |
-0.37 D |
No Change |
| +8.50 D |
+8.16 D |
-0.35 D |
No Change |
| +8.00 D |
+7.68 D |
-0.32 D |
No Change |
| +7.50 D |
+7.20 D |
-0.30 D |
No Change |
| +7.00 D |
+6.72 D |
-0.28 D |
No Change |
| +6.50 D |
+6.24 D |
-0.26 D |
No Change |
| +6.00 D |
+5.76 D |
-0.24 D |
No Change |
| +5.50 D |
+5.28 D |
-0.22 D |
No Change |
| +5.00 D |
+4.81 D |
-0.20 D |
No Change |
Tabla de correlación del Poder del lente colocado en el BAG o en el SURCO, publicado por Warren HILL.
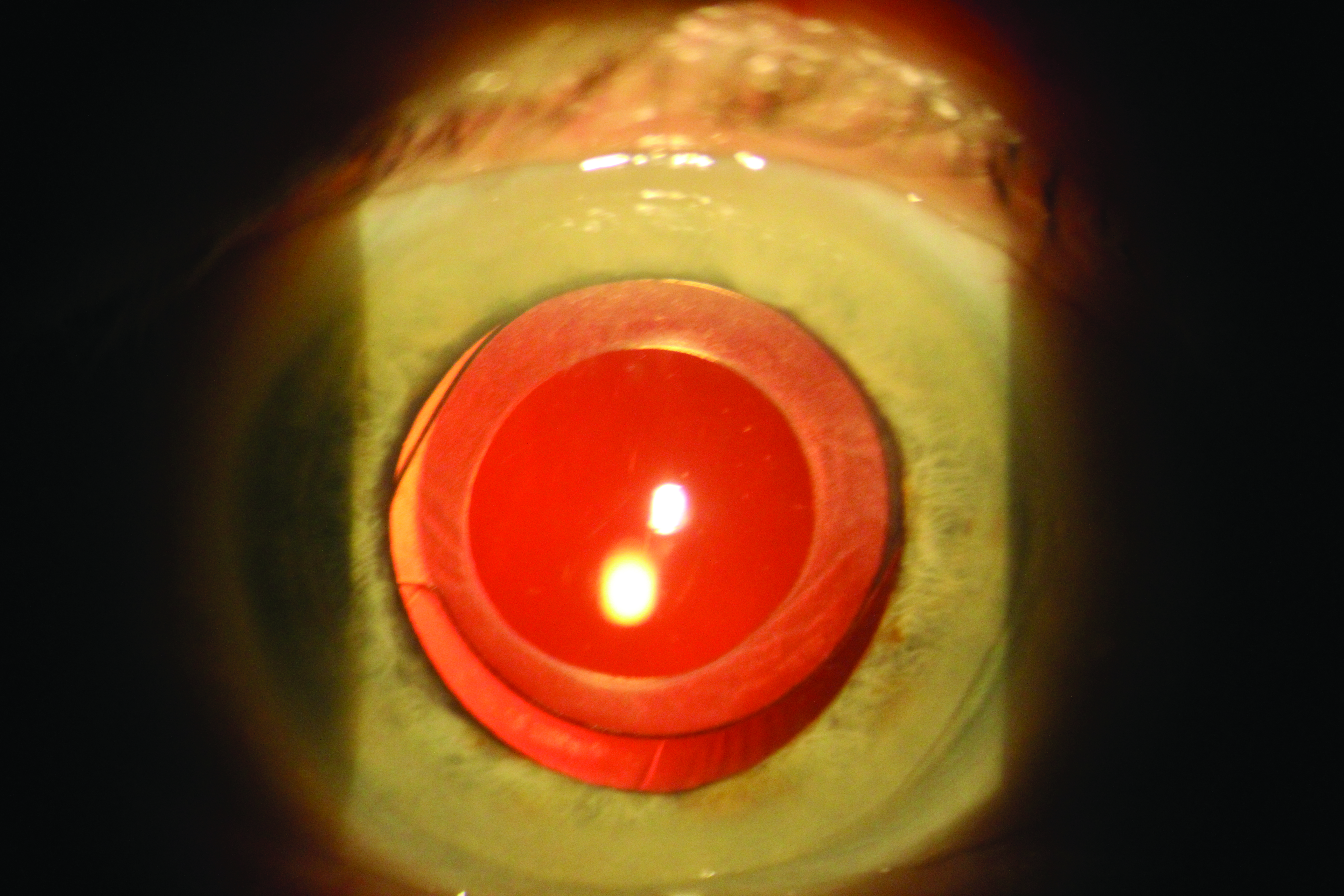
Capsulorrexis circular continua
PRIMERA ETAPA EN EL CÁLCULO DEL LENTE INTRAOCULAR
El cálculo del poder de la lente constituye un tema apasionante. Como en otras ramas de la ciencia es un encadenamiento de sucesivos e incansables intentos, con logros y fracasos. Durante años, la evolución y adquisición de tecnologías fueron condicionantes de los progresos alcanzados.
Al principio el cálculo se realizó con el Standard Lens Method, que consideraba un valor de 18 D al que se le debía sumar la refracción preoperatoria, modificada por una constante que fue calculada en 1.49.
De esta manera a un paciente con una refracción preoperatoria de +2.5 D, le correspondía un lente de 18 + (+2.5 x 1.49) = 21.725 D, y otro con – 2.5, le correspondía una de 18 + (-2.5 x 1.49) = 14.275 D.
Este método fue muy útil mientras no existieron métodos que permitieran medir el ojo con precisión, pero generaba errores debido al desconocimiento de la refracción previa, antes de la catarata, a la miopización generada por cataratas nucleares, o demás dificultades como cataratas completas, subcapsulares posteriores o corticales densas.
La historia del cálculo del LIO más exacto comenzó a partir del momento en que se desarrollaron métodos para obtener algunas dimensiones del ojo, como el ecómetro y el desarrollo de fórmulas de cálculo, teóricas o regresivas, con las que se pudiera obtener el poder del LIO más exacto.
Las fórmulas de primera generación fueron un grupo de ecuaciones matemáticas que cambiaron la historia de la carrera hacia la emetropía.
El primer eslabón de la cadena fue el ruso Svyatoslav Fyodorov2, quien en 1967 presenta su primera fórmula teórica para calcular el poder del LIO en la cirugía de catarata. Basado en óptica geométrica, utilizaba medidas ecográficas y queratométricas por primera vez. Fue un verdadero pionero, que comenzó utilizando los lentes intraoculares fabricados en Inglaterra por la firma Rayner, pero muy rápidamente comenzó a fabricar sus propias lentes Fyodorov-Sputnik (Medexport URSS) en la Unión Soviética.
En la década del 70 otras fórmulas teóricas se sumaron como la de Colenbrander 3, en 1973 para la colocación de los LIOs Iris clip que se utilizaron en esa época, o la de Van der Heijde5, en 1975 para el cálculo de LIOs de cámara anterior tipo Iris Claw, o la de Binkhorst6, en 1975, que fue diseñada para LIOs pre pupilares y retro pupilares. Todas estas últimas basadas en óptica geométrica y utilizando constantes del ojo esquemático.
Aunque aparentemente diferentes, todas estas fórmulas son de hecho idénticas, difiriendo sólo en algunos pequeños factores de corrección.
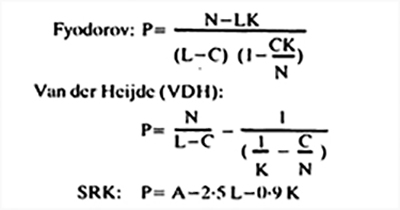
Primeras fórmulas del Cálculo del Lente intraocular
P= Poder del LIO para emetropía, N= índice refractivo del vítreo y acuoso, C= Profundidad estimada de la cámara anterior post operatoria en mm, L= Largo axial en mm, K= Poder corneal en dioptrías. A= Constante del LIO.
Todo este desarrollo de las fórmulas teóricas coincide con el desarrollo de los ecógrafos.
En 1974 Hoffer y Karl Ossoinig crean el Santa Mónica Lens Calculator Laboratory, equipado con un Ecógrafo Kretz que fue muy utilizado en esos años, sólo realizaba ecografía modo A, y contribuyó a mejorar, de manera significativa el resultado refractivo post operatorio en la cirugía de catarata.
Durante más de tres décadas fue el método más exacto y, por ser un método muy operador dependiente, estimuló a los ecografistas a perfeccionar sus mediciones, e intentar ser cada día más exactos. Esta pretendida exactitud era la resultante de una suma de errores en la medida y en las fórmulas, que se combinaban de una u otra manera, compensándose, obteniendo entonces un resultado mejor, o sumándose, y así generando errores más grandes en la refracción post operatoria.
En 1982, Donald Sanders, John Retzlaff y Manus Kraff, basados en 2500 pacientes operados crean la primera fórmula regresiva, la famosa SRK que durante muchos años fue la elegida para el cálculo del poder del LIO. (En el libro publicado por Marvin L. Kwitko y Charles Kelman, The history of modern catarat surgery, hacen referencia a una fórmula de regresión, previa a la SRK, que hizo en 1975 Thomas Lloyd, un técnico que trabajaba con James Gills, pero que no fue muy difundida).
Numerosos trabajos fueron publicados en esa época para calcular el error refractivo de diferentes fórmulas y, en general, la SRK funcionaba mejor que las teóricas y el método estándar, como el trabajo siguiente.
|
Error Refractivo Postoperatorio (Menezo y col 1984) 12 |
|
Entre ± 1D |
Entre ± 1 y 2 D |
Entre ±2 y 3D |
Entre ±3 y 4D |
Mayor a ± 4 D |
| SRK |
48,45 % |
28,64% |
10,90% |
6,36% |
5,65% |
| Fyodorov |
30,44% |
21,62% |
18,36% |
15,73% |
13,48% |
| Standard Method |
16,25% |
22,65% |
26,48% |
20,31% |
14,31% |
SEGUNDA ETAPA EN EL CÁLCULO DEL LIO
Los factores que más inciden en el cálculo del poder del LIO son: el poder de la cara anterior de la córnea, el largo axil (AL) del ojo, y la posición en la cual queda ubicado el lente luego de la cirugía (ELP). Este último parámetro es algo más complejo de calcular porque depende de dos factores, uno relacionado al lente y otro que depende del ojo del paciente. El relacionado con el LIO depende del tipo de perfil del LIO, pues existen LIOs con el poder en la cara anterior y otros en la posterior, estos últimos requieren más poder que los primeros.
El componente del ELP que depende de factores relacionados con el paciente es en función de las dimensiones del ojo, no solamente del largo axial, y de la geometría del cristalino, que hace que un LIO pueda ubicarse ligeramente anterior (resultando en una miopía) o posterior (hipermetropía). La posición final del LIO está principalmente determinada por la posición del Ecuador del LIO y el espesor del cristalino.
En base a estos elementos las fórmulas fueron perfeccionándose, así aparecieron las de segunda generación que introducen algunas variantes, como la SRK-T (1990), que optimiza la ACD post operatoria, introduce un factor de corrección del espesor retinal, ya que el largo axial que mide el ultrasonido es hasta la membrana limitante interna y el que debería ser medido es hasta la capa de conos, y también del índice de refracción corneal.
La aparición de esta fórmula de regresión hace caer en desuso la vieja SRK y la modificada SRK II, ya que vimos la poca predictibilidad, inadmisible, sobre todo en la era de la cirugía facorrefractiva.
El hecho fundamental es que la posición efectiva del lente no es directamente proporcional al largo axial.
Jack Holladay en 1995 lanza su fórmula teórica que se conoce como Holladay I que es una de las cuatro fórmulas que incorpora el IOLMaster 500. En 1997 presentó la fórmula Holladay II, un software que no tiene acceso libre y es de licencia paga. Esta última fórmula apareció como la más exacta en la época.
El australiano Graham Barrett, en 1993, lanza su fórmula universal, que no tiene la repercusión en nuestro medio que, más adelante tendrá su versión II.
Jack Holladay publica en 2006 una comparación entre las fórmulas 1 y 2 con SRK T y Hoffer Q, donde se observan los resultados, que funcionan muy similar en largos axiales de 30 a 22 mm, pero donde se separan las curvas de la Holladay 2 que se acerca a un error menor a 1 D, mientras las restantes en ojos cortos menores a 22 mm generan errores refractivos de hasta 5 D.
Alrededor de finales del milenio, se produjeron dos hechos tecnológicos que modificaron dramáticamente el cálculo del poder intraocular.
En 1999 se presentó el IOLMaster en el Congreso de la ESCRS de Viena. Curiosamente en este evento se celebró el cincuenta aniversario del primer implante de Harold Ridley, quien fue homenajeado en la ceremonia inaugural de la que tuve el inmenso privilegio de ser testigo.
La aparición de la interferometría óptica es un hito en la búsqueda de la emetropía.
El principio de la biometría óptica está basado en los estudios del físico alemán Albert Michelson y que le valieron el Premio Nobel en Física en 1907. El Interferómetro de Michelson crea un par de haces coherentes de luz infrarroja de 780 nm de longitud de onda y de aproximadamente 130 micrones de diámetro. Estos haces se logran a partir de una fuente única que incide en un espejo del que surgen los haces coherentes.
El IolMaster (Zeiss) es un método de no contacto, en el cual un haz de láser coherente de 160 μ, infrarrojo, con una longitud de onda de 780 nm, incide a través de los tejidos desde la córnea hasta el epitelio pigmentado subfoveal.
El examen resulta más repetible y exacto que con el ultrasonido, el error es de 0.02 mm, cinco veces menor que el ultrasónico, requiere una menor curva de aprendizaje y es menos operador dependiente que la ecometría, con una gran ventaja, además, que es la de disponer en un único aparato de todas las mediciones, y con la posibilidad de almacenar los estudios en la memoria.
Una ventaja extra es la de poder incorporar, en su base de datos, todas las constantes para cada lente intraocular de todas las fórmulas que incluye en cada modelo. Esto permite una presentación de los resultados mucho más amigable, teniendo en sóla una hoja los datos deseados de las cuatro fórmulas para un modelo específico de lente (multifórmula). También se puede elegir una fórmula y cuatro modelos de lentes en una hoja. Otra ventaja es la de elegir la refracción post operatoria deseada.
Esta base de datos de los lentes intraoculares y sus constantes se puede actualizar manualmente o descargando desde la página de ULIB (User Group for Laser Interference Biometry), es posible incorporar nuevos lentes, dar de baja lentes que han dejado de fabricarse o que no vamos a utilizar.
Todas estas condiciones explican el por qué considero que cambió la historia del cálculo del LIO.
Si bien existen limitaciones en algunos pacientes, en los cuales no se puede realizar, como en todos los casos de opacidad de medios, cataratas completas, subcapsulares, polares, etc. el porcentaje de los casos que quedan sin poder ser medidos es muy bajo. Este número de casos podemos disminuirlo más, aún, midiendo de rutina a los pacientes antes de desarrollar la catarata, en estadíos en los que quizás no es quirúrgico, en los pacientes que van a ser sometidos a vitrectomía (y pueden desarrollarse cataratas por aceite de silicón o gas).
Simultáneamente en esta época acompañaron algunos avances en la fabricación de las lentes intraoculares, la aparición de las tóricas y las multifocales, que significaron un beneficio importantísimo para los pacientes en el camino hacia la emetropía.
Hasta el lanzamiento de los lentes tóricos, el manejo del astigmatismo corneal estaba limitado a las incisiones arqueadas, relajantes limbares (LRI) o incisiones arqueadas a 6 mm, con una gran variabilidad en los resultados refractivos.
La alternativa a las incisiones la aportaba la cirugía con Excímer (LASIK o PRK) para corregir defectos astigmáticos o esféricos post facoemulsificación con lente intraocular (y también post lente fáquico de cámara posterior) que fue descripto por primera vez por Roberto Zaldívar y que se conoce como Bioptics48-50.
La utilización de los lentes tóricos requirió el desarrollo de un elemento diagnóstico imprescindible: el topógrafo corneal.
Además, fue necesario que cada cirujano conozca fehacientemente su astigmatismo inducido para cada tipo, localización y tamaño de incisión de manera muy precisa.
Apareció concomitantemente una herramienta que se transformó en algo habitual para nuestra práctica como son hoy día los calculadores online, originalmente provistos por la empresa fabricante de cada lente, que consideraban exclusivamente la cara anterior de la córnea, pero que luego de un tiempo de utilización, fueron reemplazados por otros más precisos, que consideraban, también, la participación de la cara posterior en el astigmatismo refractivo corneal.
El Barret toric calculator es hoy, quizás el más utilizado para calcular los lentes tóricos y resulta muy preciso.
La fórmula de Haigis optimizada, que introduce tres constantes (a0 a1 a2) y la medición de la profundidad de la cámara anterior (ACD) mejoró la exactitud del cálculo al mejorar la estimación de la posición en la que se supone quedaría el lente (ELP). En efecto, en un estudio de 2017 53 que estudia los parámetros preoperatorios utilizados en predecir la posición estimada del lente: edad, ACD, espesor del cristalino, largo axial, White to White, curvatura corneal y cómo se correlacionan con la posición en la que efectivamente quedaron los lentes intraoculares de 100 pacientes en donde se implantaron un monopieza en un ojo y un 3 piezas en el congénere, se encuentra que la ACD correlaciona mucho y el largo axial en menor medida, mientras el resto de los parámetros no correlaciona.
Debemos recordar aquí otra contribución importante de Wolfgan Haigis como fue la optimización de las constantes de todos los lentes intraoculares que se optimizaron, a partir de la participación de varios cirujanos del mundo que enviábamos los resultados de casos y que él, personalmente respondía los mails y que funcionó perfectamente hasta su retiro en 2015.
La lista de constantes optimizadas es accesible para todos los oftalmólogos en la página de ULIB (User Group Laser Interference Biometry), pero la última actualización fue en octubre de 2016.

Comparación del error medio refractivo de cuatro fórmulas. Holladay 2006
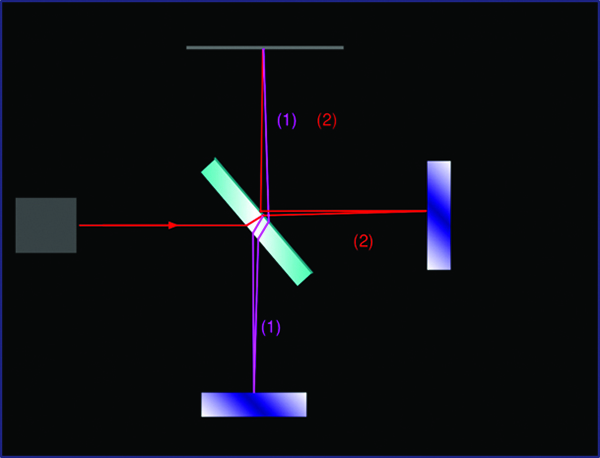
Esquema de haces coherentes de la biometría de interferometría óptica.

IOLMaster 500

Restor tórico
TERCERA ETAPA EN EL CÁLCULO DEL LIO
En esta etapa, que es la que estamos transitando, los elementos tecnológicos involucrados son otros, por un lado, la aparición de la biometría de coherencia óptica con Swept Source OCT en los últimos modelos: el IOLMaster 700 Eye Suite y el Lenstar 900 Eye Suite, que introducen un avance notable en la medición del astigmatismo, al incorporar un topógrafo y mejorar el método en la medida queratométrica y, a la incorporación del OCT que puede medir el espesor del cristalino real.
Esto permite realizar la fórmula de Olsen y Barrett universal II.
El Lenstar 900 (Haag-Streit) es un equipo que incorpora novedades tecnológicas importantes: la dual zone keratometry, con 32 medidas queratométricas que mejoran la medición del astigmatismo, la T Cone Toric Platform, que incluye una topografía corneal, que brinda imágenes (no sólo números) para confirmar el eje y poder del astigmatismo, así como también su simetría o asimetría.
El OCT permite medir el espesor del cristalino, dato necesario para utilizar la fórmula de Olsen, e incluye el Toric Planner y el Barret Toric Calculator, además del método Hil-RBF y las Fórmulas de Shammas y Masket para el cálculo en ojos post cirugía refractiva que no requieren datos históricos preoperatorios.
La ventaja de tener en un solo equipo todas estas funciones lo hace una herramienta muy eficaz.
La fórmula del noruego Olsen, es novedosa ya que las fórmulas tradicionales estiman el espesor del cristalino con la edad del paciente. La inexactitud de la ELP, como sabemos, es la mayor fuente de error en el cálculo del poder del lente Intraocular según Norrby52. La fórmula de Olsen usa el concepto de la constante C y describe la ELP como una función entre la ACD y el espesor del cristalino (LT). Como este dato trabaja independientemente de los factores tradicionales: Longitud axial, queratometria (K), white-to-white, poder del IOL, edad, o género. Por esto puede funcionar en cualquier tipo de ojo.
El IOLMaster 700 (Zeiss) con Swept Source OCT tiene varias ventajas sobre el modelo anterior. El contar con un OCT, permite detectar si el haz que está midiendo el largo axial está bien orientado hacia la mácula. Cuando se encuentra bien alineado, se puede observar la concavidad anterior que es la fóvea y corregir el punto de fijación si la imagen es recta, lo que significa que no está orientado hacia la fóvea.
Además, permite detectar irregularidades anatómicas del ojo, como tilt del cristalino, subluxaciones, etc. Mide mejor el astigmatismo que el modelo 500, ya que explora 18 puntos. Incluye la Barrett Suite que comprende el Barrett Toric Calculator para los lentes tóricos, la fórmula Barrett universal II, la Barrett true K para el cálculo post cirugía refractiva.
Se conecta directamente con Calisto (Carl Zeiss Meditec), que es una plataforma de evaluación y asistencia en el quirófano para marcar correctamente el eje en el que debemos alinear el LIO tórico, similar al Verion (Alcon)..
Existen en la actualidad algunos equipos más que utilizan la tecnología de Swept Source OCT, como el Argos (Movu) que ha sido premiado en el 2017 en la categoría en Estados Unidos, debido a su rapidez en la toma de medidas y la facilidad de manejo. Es un equipamiento muy exacto, comparado con los otros anteriormente descriptos, y tiene una ventaja sobre aquellos que es la visualización en tiempo real de la medida del largo axial en el OCT en 2D, una mayor facilidad en atravesar cataratas más densas y una exactitud comparativa con los otros equipos en todas las dimensiones medidas en un estudio sobre 107 ojos55.
Otro equipo que incorporó una unidad de biometría óptica para medir largo axial es el Pentacam AXL (Oculus), que incluye un calculador de LIO con fórmulas estándar, post refractivas y para lentes tóricas. Estas mediciones se le agregan a los que tienen los modelos anteriores Pentacam y Pentacam HB: imágenes del segmento anterior de alta resolución, mapas topográficos axiales y tangenciales, poder refractivo corneal total, mapas paquimétricos, de elevación anterior y posterior, análisis de frente de onda con análisis de los polinomios de Zernike, medidas del ángulo de la cámara anterior, su profundidad y volumen, densitometría del núcleo del cristalino con clasificación automática de la opacidad (Pentacam® nucleus staging PNS), el Holladay Report con lecturas K equivalentes, detección de queratocono y estadío. Como podemos ver, la versatilidad y multiplicidad de aplicaciones de toda esta tecnología evoluciona en una manera que los convierte en herramientas auxiliares de la cirugía de catarata y refractiva. Por ejemplo, el valor del PNS, que varía de 0 a 5 se correlaciona con el tiempo efectivo de facoemulsificación (EPT).
En esta etapa del cálculo del LIO apareció, también el calculador online para los pacientes con cirugía refractiva previa. El calculador está disponible en la página de la ASCRS y permite utilizar, si disponemos los distintos datos necesarios, las diferentes fórmulas para estos casos: Barret true K, Haigis L, Shammas, Masket, Wang-Koch-Malloney, etc.
Otra tecnología actual para el cálculo del LIO es la aberrometría de frente onda intraoperatoria que realiza el ORATM System con Verifeye+ Technology (Alcon).
Este equipo se instala en el microscopio quirúrgico y tiene como funciones, verificar y guiar al cirujano luego de la extracción del cristalino. En efecto, el ORA calcula la refracción resultante en el ojo afáquico con viscoelástico listo para implantar el lente; verifica y calcula, el poder esférico de la lente a implantar, y guía el eje del tórico en función del cilindro resultante, aconsejando si debe rotarse, y cuánto debe rotarse, o si ya está correctamente alineado, y no debemos rotarlo.
En un estudio comparativo 37 en el 89% de los casos en que se utilizó el ORA, el astigmatismo residual post operatorio fue de ± 0.50 D, versus 76% con el método estándar (P=0.006), mientras el promedio del error del cilindro refractivo fue 0.29 D vs 0.36 D respectivamente (P=0.41).
En los casos con cirugía refractiva previa ha demostrado un error refractivo medio de 0.43 D vs 0.77 D sin su utilización, con una P=0.03, comparando casos medidos con ORA, intraoperativamente, y con biometría óptica previa 39.
Otro estudio en ojos miopes, en los que compara la aberrometría de frente de onda intraoperatoria y la medida previa con varias fórmulas, también es más precisa, aún con la de Hill-NBF43.
Existen todavía controversias sobre su real beneficio para conseguir un resultado cercano a 0, una crítica que se realiza a este método es que puede ser modificable según el tipo de viscoelástico que se utiliza38 siendo mayor el error medio absoluto con Amvisc Plus y DiscoVisc.
Otras críticas tienen que ver con que existen variantes según cuánto se inyecta del viscoelástico, la presión ocular que se alcanza y si esto modifica el largo axial y la posición de la cápsula posterior, y por consiguiente en qué posición va a quedar finalmente.
Las críticas también alcanzan a un tema no menor, ya que puede generar problemas operativos en cuanto a disponer de un stock muy grande de lentes para modificar el cálculo previo a la hora de implantar un lente diferente al previsto en el examen preoperatorio.
En la actualidad se ha incorporado otro concepto de fórmula para calcular el poder del lente intraocular. Hasta este momento, las fórmulas utilizadas desde las primitivas eran dos tipos de ecuaciones: las teóricas, basadas en principios de física óptica sobre el ojo teórico y, por el otro lado las regresivas que utilizaban constantes que modificaban variables mensurables.
A partir de estas fórmulas hemos obtenido muy buenos resultados en el rango de ojos con largos axiales normales, cámara anterior normal y radios de curvatura normales, pero, cuando las dimensiones se apartan de esos valores promedio, los resultados comienzan a variar mucho entre las diversas fórmulas y el error refractivo medio es mayor y con más dispersión de los mismos. En este contexto, se comenzó a utilizar otro tipo de ecuaciones basadas en inteligencia artificial con las cuales se pueden manejar una cantidad inmensa de datos, encontrando relaciones no lineales, que son las que no utilizan las fórmulas tradicionales, entre los parámetros que medimos y dan sugerencias de qué poder de lente sería el más aconsejable para alcanzar la emetropía.
Este método da lugar a la fórmula Hill-RBF (de Warren Hill y basado en Radial Basis Function) que utiliza patrones de reconocimiento basado en inteligencia artificial e interpolación de datos.
Proviene de un gran número de casos, originalmente 3400 y actualmente más de 12000 casos, en los cuales se conocen la biometría y los resultados refractivos, en los que RBF es capaz de encontrar distintos patrones en una nube de datos random de ese universo. Los casos originales fueron medidos con el Lenstar 900 y los lentes utilizados los Acrysof SN60WL.
El calculador online (rbfcalculator.com) es de uso universal, se puede acceder desde la página web del Dr Warren Hill.
Los primeros resultados comparativos publicados muestran, en los ojos cortos, una mejor performance de la fórmula Hill RBF con un resultado en ± 0.5 D del 84.5% de los casos, seguido por 81% la fórmula de Olsen (sobre 58 casos) y en otro estudio en ojos miopes de largos axiales superiores a 25 mm la aberrometría intraoperatoria de frente de onda con la fórmula de Hill-RBF demostró ser significativamente más exacta que los cálculos preoperatorios con otras fórmulas43.
El futuro nos dirá si la medición intraoperatoria, con ésta u otra tecnología, será el método con el cual calculemos los lentes intraoculares y si las fórmulas serán algunas de las que hoy estamos utilizando o continuará esta evolución constante que viene ocurriendo en los últimos 50 años.
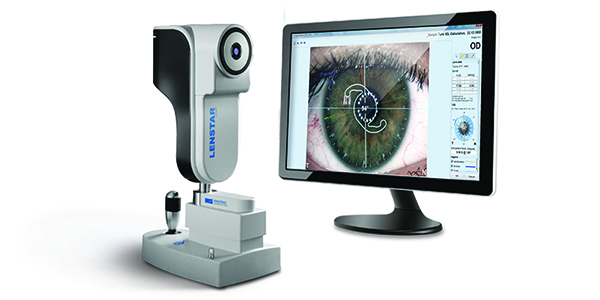
Lenstar (Haag Streit)
CÁLCULO DEL LENTE EN CASOS ESPECIALES
Existen algunos casos especiales en los cuales las fórmulas desarrolladas previamente no funcionaron, y provocaron sorpresas refractivas indeseadas. El caso emblemático es en los pacientes post cirugía refractiva. En 1990 comenzaron a aparecer cataratas en pacientes operados con queratotomía radial previa. Los errores refractivos y la fluctuación del error refractivo en los primeros meses post operatorios se convirtieron en algo habitual en nuestra práctica.
La imposibilidad en ese momento de poder medir el poder corneal central generaba hipermetropía, si se colocaba el lente con los datos de las fórmulas sin modificaciones.
Los errores se generan por varios motivos: primero porque la queratometría en córneas normales estima otro poder corneal central, en cambio en éstas el centro es de menor poder; otro que, considerando una K muy plana, infiere que la ELP estaría más adelante.
Aparecieron las fórmulas doble K, como la de Aramberri, que obligaba a conocer datos preoperatorios como la K previa a la cirugía refractiva, que se utiliza para calcular la ELP y la K actual para el resto de la fórmula. También era necesario conocer cuál había sido la corrección miópica alcanzada por el procedimiento. Cuando ocurrieron los primeros casos de post cirugía por sustracción tisular (LASIK; LASEK; PRK) se le sumaba otro error en cuanto al adelgazamiento corneal provocado. Las fórmulas de doble K fueron útiles en ese primer momento, como la de Holladay Doble K.
En 2008, Haigis publica su fórmula Haigis L 56, que genera un radio de curvatura corregido por una ecuación donde se introduce el valor de la media de la curvatura y ese resultado es utilizado por la fórmula Haigis como el radio de curvatura verdadero. Es decir, las fórmulas Haigis L y Haigis son iguales básicamente, la única diferencia es que la L miope calcula previamente una K diferente para evitar la hipermetropía.
Con el auge de los calculadores, la página de la ASCRS nos brinda una serie de herramientas de cálculo muy buenas (www.ascrs.org/online-tools). Para estos casos, el Post-Refractive IOL calculator, desarrollado por Warren Hill, Douglas Koch y Li Wang es hoy imprescindible a la hora de operar un paciente con cirugía refractiva previa.
Hay tres diferentes grupos de fórmulas: para LASIK/PRK miópico previo; LASIK/PRK hipermetrópico previo y para queratotomía radial previo.
Incluyen fórmulas que requieren datos previos a la cirugía refractiva y otras que no lo requieren.
A modo de resumen en la tabla siguientes se exponen las fórmulas y métodos que podemos utilizar para calcular en estos casos desafiantes.
| LASIK/PRK Miopico Previo |
LASIK/PRK Hipermetropico Previo |
Queratotomia Radial Previa |
| CON Datos previos |
SIN Datos previos |
CON Datos previos |
SIN Datos previos |
SIN Datos previos |
| Adjusted EffRP |
Wang Koch Maloney |
Adjusted EffRP |
EyeSys EffRP |
| Adjusted Atlas 9000 |
Shammas |
|
Shammas |
Average Central Power |
| Adjusted Atlas Ring Values |
Haigis L |
|
Haigis L |
Atlas 1-4 |
| Masket formula |
Galilei |
Masket Formula |
Pentacam |
| Modify Masket |
Potvin-Hill Pentacam |
Modify Masket |
IOLMaster/Lenstar |
| Adjusted ACCP/ACP/APP |
OCT |
|
OCT |
OCT |
| Barrett true K |
Barrett true K |
|
|
| No history |
Barrett true K |
Barrett true K |
|
| no History |
Barret True K |
|
|
Los métodos desarrollados en la página de la ASCRS, surgen diferentes fuentes de datos de distintos topógrafos, variados algoritmos, ecuaciones más o menos complejas, fórmulas teóricas, biómetros, etc.
- Adjusted EffRP: Método originado en los estudios de Koch y Wang, ajusta el poder utilizando el effective refractive power del Holladay Diagnostic Summary del Eye Sys Corneal Analysis System. Este valor es luego reducido 19% por cada dioptría de miopía corregida. Así se obtiene el valor de K con el que se calcula el lente intraocular.
- Adjusted Atlas 9000: Modificación de un método de Wang, Booth y Koch 2004, donde se toma del topógrafo Zeiss Humphrey Atlas 9000 el valor de la zona de 4 mm – (corrección en la refracción x 0.2) = K que se va a usar en el post lasik con la fórmula de Shammas.
- Adjusted Atlas Ring Value: La K se obtiene promediando el O mm, 1 mm, 2 mm y 3 mm de los anillos del Atlas 992-995 series. Este valor se modifica como el anterior.
- Masket Formula: Obtiene el poder del lente calculándolo con la K post lasik + (corrección refractiva x 0.326) + 1.01 = poder del lente a implantar.
- Modified Masket: W. Hill presenta una modificación de la anterior multiplicando por 0.4385 la corrección de la refracción y sumando 0.0295.
- Adjusted ACCP/ACP/APP: El ACCP, promedio del poder central de la córnea de los anillos de Placido dado por el Tommey, es restado por (corrección refractiva x 0.16) = K Post Lasik/PRK para calcular el LIO. ACP Mangellan y APP del OPD scan III Nidek se pueden utilizar con la misma fórmula.
- Barrett True K: Es una fórmula teórica presentada en el ASCRS de 2009, requiere el dato del cambio refractivo producido por el LASIK/PRK.
- Método de Wang, Koch, Maloney: Utiliza el (valor de K Atlas 4 mm x 1.114) – 5.59 D = K que va a utilizar en fórmula de Shammas PL.
- Método de Shammas: Utiliza un análisis de regresión, de acuerdo a éste (Kpost x 1.14) – 6.8 = K a utilizar para el cálculo del poder con la Shammas PL. La K post era el promedio del IolMaster.
- Haigis L: Usa un radio corregido que surge de 331.5 / (-5.1625 x radio medido +82.2603-0.35). Ese radio corregido es con el que se calcula el poder en la Fórmula de Haigis con las constantes a0 a1 a2.
- Galillei: Wang y Koch, usando el TCP (Ray traced) de los 4 mm centrales. El post LASIK/PRK central power es igual a 1.057 x TCP-1.8348.
- Potvin Hill Pentacam: Publicado en 2015, utiliza un análisis de regresión con TNP Apex Zone40 del Pentacam AXL, también LAxial y ACD, con la fórmula de Shammas PL
- OCT: Utiliza los valores de net corneal power, posterior corneal power, central corneal thickness obtenidos con el Optovue RTVue o RTVueXR. ACD y Largo axial son medidos con el IOLMaster.
- Barrett True K NO History: Fórmula teórica presentada en 2009 en ASCRS no requiere ninguna información previa.
- EyeSys EffRP: Fang, Hill, Wang y Koch presentaron este método en 2007. Utilizan el effective refractive power del resumen diagnóstico de Holladay del EyeSys Corneal Analysis system.
- Average Central Power: Usa el poder central de otros equipos.
- Atlas 1-4: El poder corneal promedio es obtenido promediando los anillos de 1, 2, 3, 4 mm en el Numerical View del Zeiss Humphrey Atlas Topographer.
- Pentacam: Utilizando el poder del LIO resultado del cálculo con Holladay 1 (PWR_SF_40), que es el poder del LIO obtenido por Holladay 1 doble K considerando K preop 43.86, y la postop es el promedio de la Sagital Front a 4 mm del Pentacam, centrado en pupila y el CT_MIN es mínimo espesor corneal medido por Pentacam. La fórmula es LIO a implantar= Holladay1 (PWR_SF_40)-4.4554+0.0084xCT_MIN.
- IOLMaster/LENSTAR: En este método se calcula con la Holladay1 doble K, utilizando una K previa de 43.86 tanto con el Lenstar o el IOLMaster.
Otro cálculo muy difícil es de las ectasias corneales. En los queratoconos, patología evolutiva en la que va aumentando la ectasia con los años, con astigmatismos irregulares la mayoría de las veces se generan muchas dificultades a la hora de calcular el lente intraocular cuando necesitamos operar de catarata.
En principio tenemos que diferenciar aquellos queratoconos que vienen demostrando estabilidad en las topografías y tienen una historia de buenas agudezas visuales con anteojos aéreos, en éstos Badoza y Cosentino han publicado buenos resultados refractivos y visuales con lentes intraoculares tóricos personalizados (Rayner)57.
Cuando la estabilidad está comprometida, el astigmatismo es tan irregular que no corrigió nunca con anteojos aéreos o existen cicatrices corneales que comprometen la visión y anticipan algún otro procedimiento quirúrgico para estabilizar la córnea, como segmentos intracorneales, queratoplastia lamelar o penetrante, la cirugía de catarata es conveniente hacerla luego de estabilizar la córnea. En estos casos los procedimientos sucesivos, aunque sean antipáticos y se quiera solucionar todo en un procedimiento, son aconsejables para acercarnos a la emetropía con más seguridad.
Luego de la queratoplastia, cuando está estable la curvatura corneal, calcularlo y hacer la cirugía de la catarata con el implante del LIO.
En cuanto a los queratoconos con segmentos intracorneales, existe un método más exacto para el cálculo que ha sido publicado por Luis Zunino, basado en el método de Mackool, que consiste en operar la catarata sin colocar el lente y luego realizar una refracción muy precisa con probines, con una distancia al vertex de 12 mm y según el equivalente esférico (EE) residual, cuando el EE es mayor a 8 D multiplicarlo por 1.75; cuando el EE es de 2 a 8 D por 1.70; y cuando el EE es menor a 2 D por 1.2. Utilizando un LIO con una constante de 118.85 óptica.
La tecnología viene en auxilio una vez más para no cometer errores en los queratoconos leves, que han pasado desapercibidos.
Sin evaluaciones corneales con topografía de Placido o de elevación, o aberrometría, o con algunos de los equipos más sofisticados que analizan con frente de onda aberraciones corneales, totales y cristaliniano, pueden no detectarse.
Por todo esto, es imperioso antes de colocar un lente intraocular multifocal, realizar estudios topográficos corneales para evitar colocarlo en pacientes con astigmatismo irregular leve o queratoconos incipientes.
Otro de los cálculos especiales incluye la situación en la cual se debe colocar un lente secundario en piggy back, es decir un lente atrás de otro.
El primer caso de colocación de dos lentes fue publicado por Gayton y Sanders58 en un caso de catarata en microftalmos cuyo cálculo daba 46D. Luego se comenzó a utilizar en la corrección de errores en pseudofaquia y pseudofaquia post queratoplastia59.
La corrección quirúrgica de los defectos refractivos en la pseudofaquia puede hacerse, con la extracción del lente original y la recolocación de otro con el poder adecuado; con una cirugía refractiva corneal que corrija el error48 o con la colocación de un segundo lente con la diferencia generada.
Cuando ha pasado pocas semanas de la cirugía de catarata el ideal es el recambio, cuando la córnea es adecuada para ser tratada con Excímer es lo menos invasivo, pero cuando ha transcurrido un tiempo y la cápsula ya está muy adherida, o cuando la córnea ya ha sido tratada previamente, la mejor elección es colocar un segundo lente. En este caso contamos con la refracción manifiesta que es sobre la cual hacemos el cálculo del nuevo lente.
Los primeros lentes diseñados como piggy back secundarios para ser implantados en el surco, que pueden ser monofocales, multifocales y tóricos, son el Sulcoflex (Rayner Intraocular Lenses) que fue el primero comercialmente disponible y el Add-On (HumanOptics). El primero es de acrílico hidrofílico con un largo de 14 mm y óptica de 6.5 mm de diámetro convexo-cóncava para ser implantado por 3 mm, con un rango de -5D a +5D el monofocal asférico, -3 D a +3 D el multifocal, que tiene una adición de +3.50 y el tórico de 1 a 3 D. El Add-On es de óptica de 7 mm de silicona convexa-cóncava, 3 piezas con hápticas de PMMA largo de 14 mm, para implantar por 3.2mm y con rangos similares al anterior.
El cálculo del lente es muy previsible, en la medida que se realice una prolija refracción59-60. Se puede hacer con la fórmula de vergencia para ojos pseudofáquicos y afáquicos que está disponible en la página web de Warren Hill (https://www.doctor-hill.com/physicians/download.htm#four).
El calculador Raytrace también es una herramienta para obtener el poder del Sulcoflex a implantar.
Un nuevo diseño de lente ha sido lanzado al mercado recientemente, el XtraFocus. Se trata de un lente con unas dimensiones similares al Sulcoflex, de acrílico hidrofóbico, con un pinole de 1.3 mm, óptica de 6 mm sin poder dióptrico, convexo-cóncavo, para ser implantado en el surco y que se implanta con el cartridge D del inyector Monarch (Alcon). El pigmento negro que impide el pasaje de la luz, permite el tránsito de la luz infrarroja, con lo cual puede examinarse el fondo de ojo con OCT y otros equipos que utilizan luz infrarroja.
Está indicado para astigmatismos irregulares: post RK, Post PK, queratocono, degeneración pellucida, traumas perforantes corneales y otras irregularidades. También como tratamiento de la presbicia en el ojo pseudofáquico.
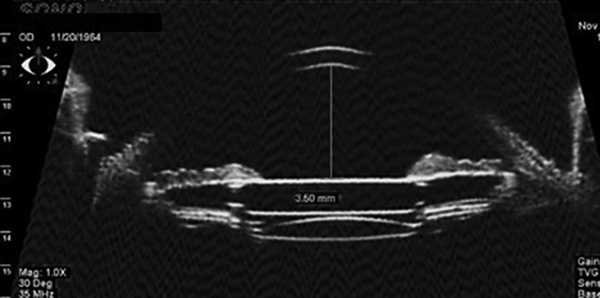
Biomicroscopia Ultrasónica de un Piggy Back
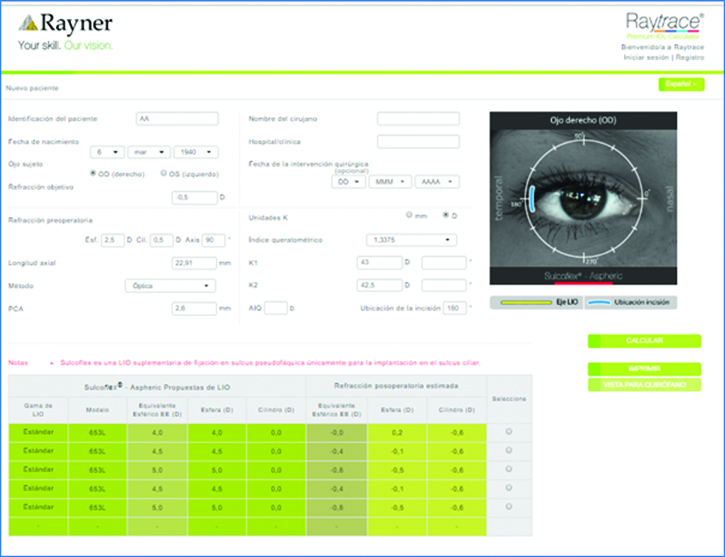
Calculador Raytrace también es una herramienta para obtener el poder del Sulcoflex a implantar.

Lente XtraFocus (Morcher)
CIRUGÍA REFRACTIVA CORNEAL
Como estuvimos desarrollando previamente, la primera aproximación para corregir los vicios de refracción fue la de modificar la forma de la córnea.
Su principal ventaja es la de no introducirnos en el globo ocular, actuar sólo en la superficie ocular y de esta manera ser un procedimiento extraocular.
En la córnea se puede actuar de distintas maneras para, modificando su curvatura, cambiar su refracción:
- Hacer incisiones (relajantes)
- Sustracción tisular
- Adición (tisular y biomateriales)
- Contracción Tisular
- Compresión Tisular
Incisional relajante: queratotomía radial, queratotomía arqueada
En 1969, en la Unión Soviética, Yenaliev, tomó los trabajos de Sato en Japón, y sin realizar las incisiones en la cara posterior revitalizó la cirugía por incisiones relajantes que se llamó Queratotomía Radial. Su casuística hasta 1977 alcanzó 426 ojos miopes de menos de 12 D. Realizó 24 incisiones en 290 ojos, 12 en 50 ojos, 8 en 30 ojos y 4 en 56 ojos.
Casi simultáneamente, Svyatoslav Fiodorov realizó, en 1974, las primeras cirugías de queratotomía radial (KR), luego de establecer nomogramas, que eran unas tablas en las que establecía qué parámetros había que elegir para corregir el defecto a operar. Estos incluían la miopía a corregir, la edad del paciente y, lo que debía hacer el cirujano, con el diámetro central libre de incisiones, el número de incisiones y la profundidad del corte.
Fiodorov también diseñó nuevos y mejores instrumentos de marcado y medición, así como los de corte, bisturíes de diamante calibrados y con tope, para hacer un corte exacto de la profundidad deseada, de acuerdo con el espesor corneal del paciente. Durante esos años Moscú fue la Meca de muchos oftalmólogos de Europa y Estados Unidos. No solamente por la cirugía refractiva, sino por su legendario quirófano en el que se realizaban las cirugías con un criterio serial similar a una planta de producción industrial.
Uno de los más entusiastas, Leo Bores introduce la KR en USA en 1978. La década de los 80 fue el cénit de la cirugía corneal Incisional. Durante 10 años surgieron nomogramas varios en las que se establecían algunos parámetros que, de acuerdo con la miopía a corregir, había que cumplir con las incisiones a realizar. La zona óptica libre de incisiones cuando más pequeña, más miopía corregía. El mínimo era 3 mm, pero luego se comprobó que hacer incisiones a 1.5 mm del vértice corneal generaba otros problemas como astigmatismos irregularidades y glare intenso. Las incisiones usualmente eran 8 radiales, que debían llegar al limbo, pero también se hicieron 16, lo que generaba una córnea mucho más inestable. Luego hubo una técnica que promovía Richard Lindstrom que se llamó Mini-RK, en la cual las incisiones llegaban a 1 mm del limbo. Esta técnica la utilizaba para miopías muy bajas y la zona óptica se limitaba a 4 mm, pues debíamos no llegar más cerca del centro visual para evitar los problemas vinculados con la presencia de incisiones en el área central.
En 1994 se publicó el PERK19 (Prospective Evaluation of Radial Keratotomy), que fue un estudio que evaluó más de 600 casos con 10 años de seguimiento. El PERK demostró que existía una tendencia a la hipermetropía de 1 D en el 43% de los casos luego de 10 años de operados. Los resultados refractivos de la RK mostraban que el 70% de los pacientes continuaban, a los 10 años, sin utilizar anteojos, la AV sin corrección era de 20/40 o más en el 85% de los casos y el 53% de los casos alcanzaban 20/20 sin corrección. El shift hipermetrópico fue la alerta para abandonar esta técnica. Por supuesto, también en esa época, el excímer comenzaba a tener resultados muy alentadores.
La queratotomía arqueada, para tratar astigmatismos, sobrevivió a la queratotomía radial que cayó en desuso cuando el LASIK se expandió masivamente.
Las incisiones transversales, arqueadas y rectas, de distintos diseños se acompañaron con incisiones radiales durante los 10 años que se utilizaron. Algunos esquemas de incisiones transversas, como las que proponía Luis Antonio Ruiz, consistían en un par de 2 ó 3 incisiones rectas transversales, más cortas las centrales y más largas las periféricas, entre dos incisiones radiales no contactantes. Eran poco previsibles en cuanto a la exactitud.
Las incisiones arqueadas, tenían ventajas sobre las rectilíneas, se realizaban a 6 ó 7 mm entre ellas, es decir a 3 ó 3.5 mm del centro del centro corneal. Existían distintos marcadores para medir el largo de cada una que podía ser de 45° a 90° de largo. Las que mejor funcionaron fueron las arqueadas solas, que corrigen astigmatismos mixtos con equivalente esférico cercano a 0 20.
Las que hoy sobreviven son las arqueadas a 6 ó 7 mm realizadas con bisturí para corregir astigmatismos regulares mixtos, como también las incisiones relajantes limbares (LRI) que se realizan a 1 mm del limbo, en conjunto con la cirugía de catarata y que actualmente, resurgieron algo por la aparición del láser de femtosegundo.
Todavía la corrección Incisional, en cuanto a la predictibilidad está lejos de la exactitud absoluta, ya que existen muchos factores que modifican la acción que este tipo de incisiones produce en la arquitectura corneal. La ubicación respecto a la distancia al vértice corneal es muy importante, pues cuanto más cerca se realizan más corrección generan. Así también, cuanto más larga y más profunda es una arqueada, más aplanan en ese meridiano, pero si bien los nomogramas establecen parámetros de corrección, influyen muchos factores de cicatrización de cada córnea, que genera una variabilidad muchas veces imprecisas. En este tema, los lentes tóricos han demostrado superioridad absoluta hasta ahora.
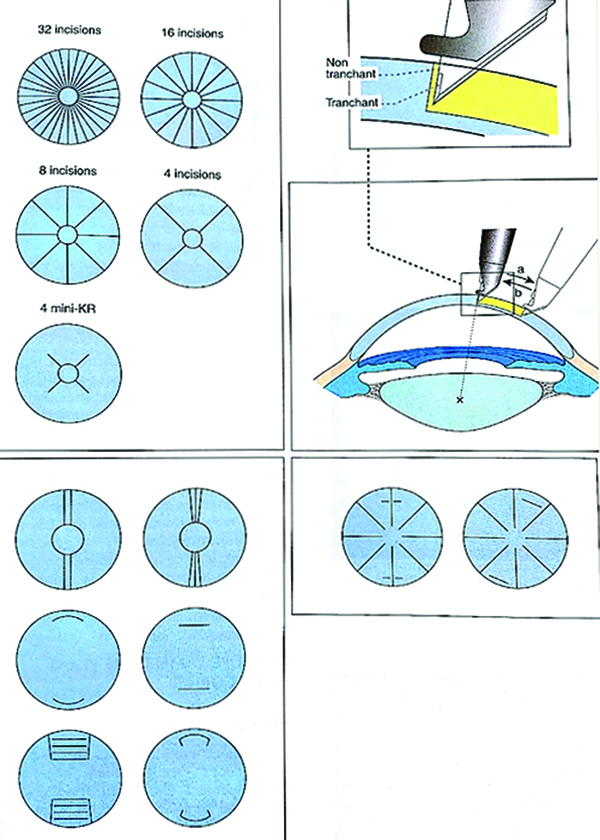
Diversos tipos de diseño de incisiones utilizadas en la Cirugía corneal Incisional.
Sustracción tisular: Keratomileusis
La sustracción del tejido corneal fue otro camino para corregir errores refractivos. La miopía, como la hipermetropía y el astigmatismo fueron tratados y siguen siendo tratados por este método en la actualidad.
La diferencia entre los dos métodos sobre la córnea estriba en que, mientras el sustractivo trata de modificar exactamente la curva de la córnea, mediante una intervención calculada matemáticamente, (como quien talla en un aparato de óptica), la incisional depende de muchos factores de la cicatrización de las incisiones que la hace más inexacta.
Barraquer estudió, experimentalmente, las modificaciones del espesor de la córnea y la curva de las superficies, las normas que rigen esta relación entre espesor y curva, la denominó “Ley de Espesores”.
En la zona adelgazada, la curva de la cara anterior disminuye, aumenta su radio y la córnea se aplana, mientras en la zona engrosada, la curva de la cara anterior aumenta, disminuye su radio y la córnea se incurva.
En queratoplastias laminares al aplicar un injerto de menor espesor que el lecho, la cara anterior de la córnea se aplana, mientras un injerto más grueso, se incurva. Estas variaciones de curva, en relación con las modificaciones de espesor, son más acentuadas cuanto menor es el diámetro del injerto, y menores, cuanto mayor es su dimensión.
Al microquerátomo original de Barraquer lo sucedieron modificaciones varias que lo trnasformaron en microquerátomo automatizado. Así nació la Keratomileusis Lamelar Automatizada (ALK), en el que un primer corte tallaba el flap superficial de un espesor de 120 micras aproximadamente y luego se realizaba un segundo corte en el lecho, de diámetro menor y cambiando el espesor de la placa, dependiendo de la ametropía a corregir, y finalmente colocando el primer flap suturado con puntos de nylon 10-0 inicialmente, más adelante sin sutura cuando se creaban flaps de corte no completo.
La aparición del Excímer Láser generó un cambio significativo e hizo caer en el olvido todas las previas técnicas de cirugía corneal Incisional o de sustracción.
El Excímer Láser fue inventado en 1970 por Nikolái Básov, V.A. Danilychev y Yu M. Popov, en el Instituto de Física de Moscú. El químico indio, Rangaswamy Srinivasan demostró en 1980 que un láser excímer es capaz de cortar y extraer fragmentos con precisión, sin causar daños térmicos a los tejidos circundantes.
Este fenómeno conocido como foto-descomposición ablativa es el que va a ser útil para la cirugía refractiva corneal, en 1985, cuando Stephen Trokel de la University of London publicó su trabajo en querotomía radial utilizando láser excímer26. Aquí ocurre una curiosidad, que es muy común en esta carrera de las tecnololgías nuevas, inicialmente se incorpora una herramienta nueva al procedimiento anterior. Durante unos años continuó estudiando el efecto y cómo se podían mejorar las incisiones radiales hechas con el Excimer27. En 1988 cambia el concepto de cirugía Incisional a sustractiva y publica un trabajo en monos donde realiza una queratectomía fotorefractiva (PRK) usando el Excimer28, este es el comienzo de la PRK, luego del LASIK:
Fue recién en 1990 cuando Ioanes Pallikaris, de Creta, publica por primera vez con el término de Láser in situ Keratomileusis (LASIK).
A partir de ese momento el excímer láser se convirtió en el procedimiento refractivo más utilizado en el mundo en la época, coincidentemente con la caída de la cirugía Incisional luego de la publicación del PERK en 1994.

Ioannis Pallikaris
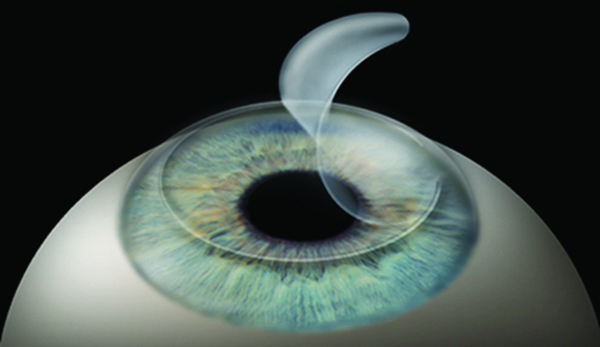
Laser In Situ Keratomileusis (Lasik)
Los desarrollos del Microquerátomo, de los distintos equipos de excímer láser y la aparición de la topografía, que permitió ver las grandes irregularidades corneales generadas por la queratotomía radial, por un lado, pero, por el otro mejorar los perfiles de ablación de los láseres, limitando las indicaciones a miopías e hipermetropía más bajas; permitiendo conocer más sobre las ectasias corneales y cómo evitarlas, contribuyeron a transformar el LASIK en un procedimiento muy exacto, seguro y masivo.
A partir de quedar confirmado el excímer, las tecnologías se dirigieron a conseguir ablaciones más perfectas, perfiles de ablación con menos aberraciones, flaps de diámetros más grandes realizados con microquerátomos con cortes más delgados y homogéneos como el Pendular de Cesar Carriazo.

Microquerátomo Pendular de César Carriazo.
Hoy día el LASIK, LASEK, PRK siguen siendo herramientas indispensables en la búsqueda de la emetropía.
En la década de los años 2000, comenzaron a utilizarse los aberrómetros y surgió una novedosa técnica de ablación, con la que hubo más expectativa que resultados reales obtenidos, la ablación personalizada. Este procedimiento consiste en ablacionar el estroma guiado por una aberrometría previa, de manera que el tratamiento corrigiera totalmente las aberraciones existentes. Durante un tiempo se utilizó con la idea de obtener la súper visión, la publicidad proponía en 2010 alcanzar 20/10, pero paulatinamente se fue dejando de lado en la medida que los resultados obtenidos no fueron los esperados.
Un procedimiento que utiliza sustracción tisular y fue muy auspicioso en su momento fue el PresbyLASIK, que consiste en tallar la córnea con el excímer, de la misma manera que el Lasik hipermetrópico o el miópico, pero creando una córnea multifocal, generando una parte central que sirviera para lejos y la periferia para cerca. Este procedimiento, que también lo realizó el Tchnolass y llamó SUPRACOR, tiene como inconvenientes principales que sólo el 65% alcanzaban 20/20 sin corrección, pero un 20% experimentaba la pérdida de 2 líneas de AV y porque existía la posibilidad de decrecer la calidad de visión por la presencia de aberraciones.
En los últimos años la incorporación del láser de femtosegundo genera un cambio significativo en la cirugía del Lasik, con la posibilidad de tallar flaps corneales sin utilizar el microquerátomo.
Esto permite la construcción de flaps ultradelgados, pero con un costo adicional por procedimiento, que plantea una controversia entre los cirujanos que todavía no justifican la introducción de esta tecnología.
No obstante, en el último año y medio, otra aplicación del femtosegundo ha ido ganando adeptos, el SMILE (Small Incision Lenticule Extraction), que es un procedimiento de sustracción tisular, pero sin excímer.
Este tratamiento puede corregir todos los defectos refractivos: hipermetropía, miopía, astigmatismo y presbicia. En 2007 comenzó a realizarse como FLEx (Femtosecond Lenticule extraction) que sería una variante del ALK, para tratar miopías elevadas.
En 2011, a partir de aquél, surge el Smile, que a través de una incisión de 2 a 3 mm extrae por completo el lentículo sin necesidad de hacer un flap como en el Flex. Los resultados, aunque todavía muy iniciales parecen muy promisorios, incluyendo algunas ventajas sobre los procedimientos que crean un flap, en cuanto a reducir la incidencia de ojo seco.
El SMILE se realiza en varios centros del mundo y fue aprobado por la FDA a fines de 2016 para el Zeiss VisuMax.
En un estudio sobre 88 ojos, Ang y col 47 encontraron un 95.5% en ±1.00 D y 78.4% en ±0.50 D de la corrección intentada y 20/40 o mejor en 100% y 20/20 en 76.5%.
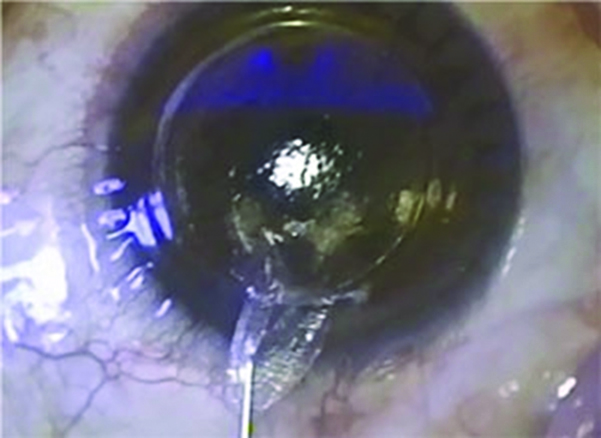
Técnica de SMILE (Foto Jesper Hjordal)
Adición tisular
La corrección refractiva mediante la adición tisular se puede realizar con tejidos biológicos, estroma de córneas de donante, o con biomateriales.
El primer grupo incluye un procedimiento que se conoció como epiqueratofaquia presentada por Kaufman en 1980, que consistía en la sutura de un lentículo de córnea, de espesor y diámetro preestablecido siguiendo la ley de espesores, luego de la desepitelización. Se utilizó para corregir miopías altas, afaquias del adulto o pediátrica, altas hipermetropías. El lentículo era tallado por congelación, según la ametropía a corregir, conservado liofilizado y comercializado por AMO. El procedimiento fue abandonado.
En cuanto a los biomateriales, en la actualidad son numerosos los procedimientos que utilizan este principio, encuadrándose en dos categorías: los inlays y los segmentos (anillos) intracorneales.
Los inlays son dispositivos que se colocan en el eje visual, actuando ópticamente o como estenopeico para corregir fundamentalmente la presbicia. En general se utilizan monocularmente en el ojo no dominante. Tienen una ventaja importante que es la reversibilidad.
Existen varios dispositivos, uno de ellos el Kamra que está aprobado por la FDA, utiliza el principio estenopeico, tiene un diámetro de 3.8 mm y una abertura central de 1.6 mm, un espesor de 5μ, el material utilizado es el fluoruro de polivinilideno, con nanopartículas de carbón, microperforado con 8400 orificios de 5 a 11 μ que permiten un flujo corneal normal. El implante en la actualidad se realiza a través del tallado de un bolsillo realizado con el láser de Femtosegundo o, en un flap realizado con el microquerátomo, a 220μ o más profundo. Puede implantarse en emétropes o luego de un lasik miópico o hipermetrópico.
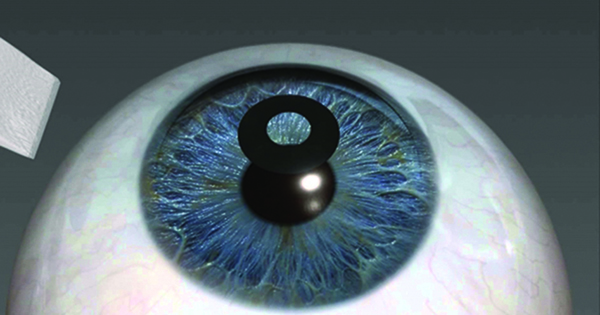
Esquema de Inlay Kamra.
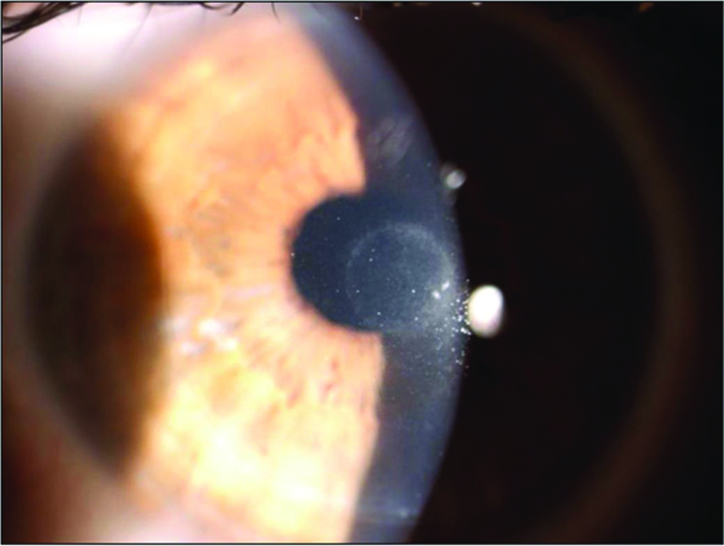
Inlay Raindrop
Otro dispositivo es el Raindrop, un implante de hydrogel transparente, permeable, un menisco positivo con un diámetro de 2 mm, con un espesor central de 32 μ con un índice de refracción similar al de la córnea. No tiene poder refractivo per se, sino que altera la curvatura en el centro, con la que modifica el poder refractivo creando una córnea hiperprolada, multifocal. El material permite un libre pasaje de oxígeno y nutrientes.
En ambos inlays es crítico el centrado. Han finalizado los estudios clínicos del Raindrop y está a la espera de la aprobación de la FDA. En estudios de satisfacción en base a cuestionarios al año de operados, el 95 % estaba satisfecho o muy satisfecho con la visión cercana e intermedia, todos reportaron estar muy satisfechos con la visión lejana.
En cuanto a los llamados anillos, que deberían llamarse segmentos, intracorneales, podemos decir que se originaron en los implantes intracorneales que comenzó desarrollando, en sus estudios sobre las características biomecánicas de la córnea, José Ignacio Barraquer.
La indicación actual es el queratocono y las ectasias corneales exclusivamente, aunque en 1991 W. Nose y Paulo Ferrara diseñaron segmentos que fueron utilizados para la corrección de miopías bajas y altas, respectivamente.
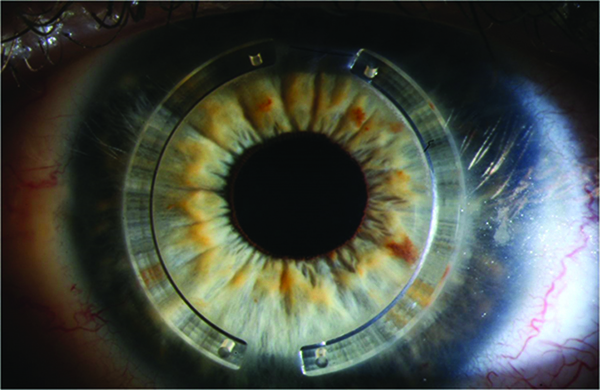
Segmentos intracorneales.
Contracción tisular
Este mecanismo de acción sobre la córnea tuvo su máxima expresión con un procedimiento que se llamó Queratoplastia conductiva (CK).
Este procedimiento, aprobado por la FDA en 2002, para tratar hipermetropías de + 0.75 D a + 3 D, consistía en aplicar de 8 a 32 spots de radiofrecuencia en uno a tres anillos de la periferia corneal. Cada uno de estos spots producía una contracción a nivel del colágeno estromal que generaba un aumento en la curvatura central por la contracción tisular producida en el colágeno estromal a nivel de los spots. Este efecto es similar al producido por el Holmium-YAG laser y se denominó Láser Termo Keratoplastia (LTK). Si bien estos procedimientos tuvieron un auge en la década del 90, estudios ulteriores demostraron una escasa estabilidad y predictibilidad, como así también la aparición de astigmatismos irregulares que hicieron abandonar el tratamiento. Otro punto por considerar es que, si bien la CK demostró ser un tratamiento bueno para la hipermetropía, la estabilidad era muy incierta. La regresión del efecto era muy frecuente. En algunos trabajos la refracción variaba de +1.49 D previo a +0.29D a los 2 años y a +1.39 D a los 73 meses30.
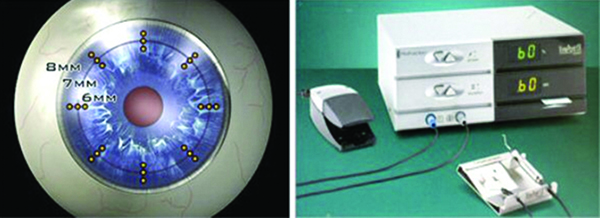
Queratoplastia Conductiva
El uso de la CK, que demostraba ser efectivo y seguro para la hipermetropía, llevó a investigaciones para el tratamiento de la presbicia. La FDA aprobó el procedimiento para realizarlo en presbicia para el ojo no dominante apuntando a una refracción de -1D a -2D. Los resultados de satisfacción inicial fueron muy buenos, pero la falta de certeza a largo plazo y la regresión bien documentada en hipermétropes ocurrió en los présbitas, en definitiva, era una solución pasajera.
CIRUGÍA FACORREFRACTIVA
El desarrollo de la tecnología en diversas variantes diagnósticas y terapéuticas, de las máquinas de facoemulsificación, de los topógrafos, de la fabricación de las lentes intraoculares (por la aparición de los lentes tóricos y multifocales) y de los métodos de cálculo del LIO (en aparatos de medición y desarrollo de las fórmulas), ha permitido la aparición de la Cirugía facorrefractiva (Refractive Lens Exchange).
Como lo exponemos anteriormente, los primeros intentos de correcciones refractivas a través de procedimientos quirúrgicos en el cristalino se originan muy atrás en el siglo XIX con Fukala, pero en ese momento la tecnología no lo acompañaba, pues no existían los lentes intraoculares, sólo era posible hacerla en miopes altos, con el consiguiente riesgo de desprendimiento de retina.
En la década del 90, luego del advenimiento de la cirugía de catarata por incisión pequeña, que venía desarrollando Charles Kelman desde 1967, sin tanto éxito pues las máquinas de faco no habían logrado un nivel de desarrollo como en esa época, hubo otro furor de cirugía de recambio de cristalino transparente en miopes altos, a partir de varios cirujanos europeos que lo propiciaban, como Joseph Colin, de Francia, quien presentaba todos los años en el ESCRS los resultados de sus procedimientos en miopes extremos, hasta que se produjo un 10% de desprendimiento de retina a 8 años de operados y abandonó el procedimiento en jóvenes y miopes altos. Su casuística está basada en facoemulsificación realizada en los años 90, con incisiones de 3.25 mm y lentes rígidas con una tasa de 61% de opacificación capsular con necesidad de Yag láser y sin tener en cuenta si tenían DPV previo.
La serie de progresos tecnológicos que permitieron esta realidad que hoy es la cirugía facorrefractiva comenzó con la aparición de lentes intraoculares plegables. Pensemos que originalmente las incisiones eran esclerales, de 3.25 mm para realizar la facoemulsificación y agrandarla para introducir la lente.
El primer lente plegable lo implantó Mazzocco, era de una pieza, en forma de plato y completamente de silicón, que se podía implantar por incisión pequeña de 3.50 mm.
El mejoramiento de las máquinas de facoemulsificacion, comenzando con la irrigación y una mejora que redujo la posibilidad de producir un colapso de cámara como la irrigación continua, la posibilidad de contar con alturas variables de la botella del BSS o Ringer lactato, actualmente con la posibilidad de generar presión positiva para compensar bruscas descompresiones, son todos avances que permitieron y permiten completar una cirugía con baja incidencia de complicaciones.

RayOne Toric
En cuanto a los avances en el módulo del ultrasonido que fueron desarrollándose en estos años comenzando con la posibilidad de modular el ultrasonido con el pedal, pues al principio se seteaba en el panel, y el cirujano tenía todo o nada, luego la aparición de modos lineales que aumentaba el poder a medida que se presionaba el pedal, fue un gran avance.
La incorporación de los modos discontínuos de facoemulsificación, como el modo pulsado y el burst, que redujeron sensiblemente el tiempo efectivo de ultrasonido y las posibilidades de quemaduras en la incisión generaron el término de faco frío. En este sentido una innovación muy importante fue la de los modos torsionales, ya que hasta el momento el tip del faco se movía sólo en el sentido longitudinal.
El Ozil fue una gran innovación que hizo más efectiva la faco, reduciendo el poder del ultrasonido longitudinal y redujo aun más el efecto térmico sobre la incisión. El desarrollo de los tips acompañó la progresiva reducción de la incisión hasta 1.8 mm.
Esta incisión reduce el astigmatismo inducido y así apareció la faco microcoaxial, los fabricantes de lentes intraoculares debieron evolucionar con los inyectores para poder utilizar esas incisiones. En la actualidad las incisiones utilizadas habitualmente en general están en 2.2 mm, que permite la introducción de la mayoría de los inyectores.
Toda cirugía que se realiza sobre el cristalino debe considerarse como refractiva, se haga sobre un cristalino transparente, como una necesidad refractiva o sobre un cristalino con una catarata importante en donde la necesidad primaria es la del restablecimiento óptico. No obstante, debemos tener en cuenta que no siempre lo mejor para el paciente es la emetropía. Es mandatorio conversar con el paciente en detalle sobre las expectativas de la cirugía y decidir cuál es el mejor resultado refractivo, cuál es el mejor lente para obtenerlo.
Como vimos anteriormente la exactitud de los primeros métodos de cálculo era muy baja. Hoy contamos con uno de los registros más grandes sobre el resultado refractivo post cirugía de catarata que lo brinda el European Registry of Quality Outcomes for Cataract and Refractive Surgery (EUREQUO), que acumula hasta hoy más de 2.000.000 de ojos tratados y cuyos resultados arrojan un 91.5% de ellos con un equivalente esférico en
±1.00 D sobre la refracción intentada.
La incorporación de la corrección del astigmatismo fue la que permitió, de manera completa, la posibilidad de corregir “todos” los defectos. Estadísticas europeas muestran que un 85% de la población estudiada tiene un astigmatismo corneal de 1 D o más44. En un principio los lentes monofocales y multifocales corregían solamente el defecto esférico, lo cual limitaba un porcentaje muy importante de la población que tiene más de 0.75 D de astigmatismo.
La invención de los lentes tóricos por Shimitzu en 1992 fue una piedra fundamental en la carrera por lograr la emetropía. En la época de Ridley no era posible pensar en corregir el astigmatismo, solamente fue posible con los avances que acompañaron todos los desarrollos ulteriores.
La mayoría de los lentes monofocales tóricos, aportan la corrección del cilindro en la cara anterior y los multifocales en la cara posterior. El cálculo del cilindro es fundamental y para esto contribuyen la topografía y los calculadores.
La alineación del cilindro se debe realizar en el meridiano positivo. Existen muchos sistemas de marcación del eje, en este sentido las tecnologías pueden variar desde un simple anillo de Mendez, un marcador de fibra de punta fina con el que pintar, en posición vertical en la lámpara de hendidura y con la hendidura horizontal, los meridianos a hora 3 y 9, para evitar los errores de la ciclotorsión que se produce con el paciente acostado. También existen dispositivos más complejos de marcación, que consiste en un instrumento con un peso, que hace que el vástago quede absolutamente vertical, y las marcas se ubiquen con precisión en el meridiano horizontal a hora 3 y 9.
Otras tecnologías muy sofisticadas, como la del Verion y Calisto, consisten en una unidad de examen en consultorio en el que se registra el reconocimiento del ojo a partir de los vasos conjuntivales, la medición del poder corneal y el eje del astigmatismo. Una vez obtenidas las mediciones adecuadas y suficientes, el software del consultorio realiza la planificación de la cirugía, es decir el cirujano introduce la incisión principal de su preferencia, o donde la planea hacer para ese paciente en particular, la paracentesis una o dos, según su elección, los datos del largo axial si es que fue medido con otro equipo no conectado con estos. El planner tiene en su base de datos las constantes de los lentes que se decidan cargar y calcula el poder, el cilindro del tórico e indica el meridiano en el que debemos orientarlo. Se guarda el plan, que se transfiere al equipo de quirófano, que está colocado en el microscopio. Luego de la calibración, el primer paso es reconocer el ojo. A continuación, se observa sobreimpresa en la imagen que vemos a través del microscopio una marca en el limbo donde hay que ubicar la incisión principal y otra en la paracentesis de acuerdo con lo planificado. Esta imagen proyectada se puede anular, desde la pantalla táctil que maneja una asistente no estéril, toda vez que el cirujano lo desee. Durante la capsulorrexis podemos ayudarnos con otra imagen proyectada que programamos en el quirófano, del diámetro elegido y centrada en la pupila o en el eje visual. Esta guía de la capsulorrexis es una buena ayuda para lograr CCC del centrado, tamaño y circularidad buscada. Si hay una ventaja que se atribuye a estos equipos es la de alinear el eje del cilindro con mayor exactitud, una nueva proyección es la encargada de mostrar el eje en el que es necesario colocar, alineadas, las marcas que tienen todos los LIO tóricos. La última proyección nos ayuda a verificar si el lente multifocal está bien centrado.
Si bien esta tecnología tan sofisticada es un auxiliar muy útil, existen algunos detalles que transforman el procedimiento habitual, haciéndolo más lento y complejo.
Los lentes intraoculares multifocales comenzaron en la década del 90 con el AMO Array, un lente refractivo, de tres piezas y óptica de silicón. Antes había habido algunos bifocales que no aportaron buenos resultados. El Array fue el primero bastante utilizado, pero los halos y la falta de una buena visión cercana contribuyó a su progresiva desaparición. AMO continuó con el mismo formato, apareció el ReZoom que también era refractivo, de tres piezas, con óptica de acrílico. La visión de lejos era buena, la intermedia aceptable, pero la cercana insuficiente.
En el año 2000 apareció un nuevo concepto que fue la óptica difractiva apodizada del Acrysof ReSTOR (Alcon) con un cambio significativo en los resultados. El primer modelo tenía una adición superior de +4, luego cambiada por la adición de +3, utilizaba la plataforma de una pieza de acrílico hidrofóbica del Acrisof IQ y el filtro amarillo. También existe la variante del modelo de 3 piezas, que se utiliza menos, pero que tiene sus indicaciones ante rupturas de cápsula posterior. Simultáneamente AMO desarrolló el Tecnis one que es una monopieza similar al ReSTOR pero sin el filtro. Este tipo de lentes funciona en general muy bien, pero en ocasiones la visión de cerca es muy buena y no tanto la intermedia, o existen algunos problemas con la visualización de los halos con las luces y disfotopsias.
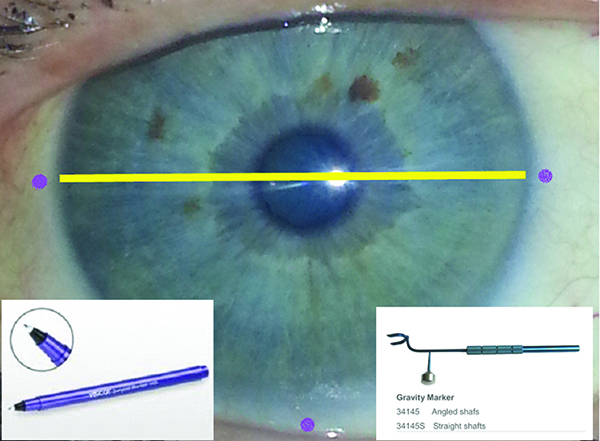
Identificación del eje horizontal con lámpara de hendidura con marcador gravitatorio o marcador de punta fina.
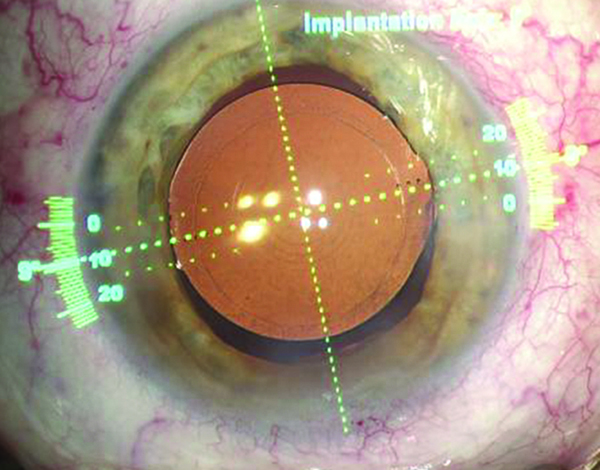
Marcado del EJE del Cilindro del Verion.
Durante más de una década estos fueron los lentes que se utilizaron para corregir la presbicia. últimamente estamos ante los lentes Trifocales y de Rango Extendido (EDOF), que incluye varios modelos que están orientados a mejorar la performance en las distancias intermedias, que es el punto débil de los multifocales.

Lente Physiol (Fine Vision)
Este grupo de lentes incluye trifocales como el Fine Vision Micro F IOL (PhysIOL) con una adición de +3.33D de cerca y +1.66D de intermedia; el AT Lisa tri (Carl Zeiss), con adicion de +3.5 D y +1.75D; el Pan Optix (Alcon), con +3.25 D y +2.17D y de rango extendido como el Tecnis Symfony (Johnson & Johnson Vision) que es un lente monopieza de acrílico hidrofóbico y un nuevo concepto de foco extendido con separación de la energía sin overlapping del foco de cerca y de lejos, es difractivo en la cara posterior y la anterior es asférica negativa (-0.21 μ).
Existen numerosos estudios que comparan estos lentes, todavía no hay conclusiones categóricas sobre sus ventajas significativas45-46.
En los próximos meses está por lanzarse un nuevo trifocal, que va a ser el primero precargado en el mercado, que va a ser de acrílico hidrofílico y es de la firma Rayner, que como vimos es el origen de todos los lentes intraoculares allá lejos en 1949, curiosidades de la historia de la evolución de las tecnologías para la emetropía.
En los últimos años, a los equipos de facoemulsificación disponibles, se agrega el Láser de Femtosegundo, que es una nueva tecnología muy útil para la cirugía de córnea, refractiva, de los anillos intracorneales y también para la cirugía del cristalino.
Es muy controvertido todavía el beneficio real que el FLACS (Femto Laser Asisted Cataract Surgery) o CICAFE (Cirugía de Catarata Asistida por Femtosegundo) aporta a la cirugía del cristalino.
Existen detractores y promotores fervientes de la cirugía con Femto. En cuanto a las acciones que el Femto láser realiza están, la capsulorrexis circular continua, la fragmentación del núcleo, las incisiones corneales principal y paracentesis, y las arqueadas para corregir astigmatismos.
El Femto láser corta el tejido a través de la foto disrupción con un haz de luz infrarroja atraviesa medios no opacos, crean un plasma de electrones libres y moléculas ionizadas, que se expanden y colapsan, generando burbujas de micro cavitación que separan el tejido de manera controlada. Cuenta con un sistema de guía con OCT en tiempo real de alta resolución, que hace que este proceso se puede hacer muy preciso.

Lente Symphony
Numerosos trabajos comparan los resultados entre la facoemulsificación manual y la asistida con láser de Femtosegundo. En cuanto a resultados refractivos, teniendo en cuenta que una de las ventajas del centrado de la cápsula y el overlaping garantizado por la capsulotomía con Femto, en un estudio retrospectivo de 1838 casos, un 82.6% de los FLACS vs un 78.8% con manual alcanzó un error absoluto de ±0.50D; 97.7% vs 97.2 % en ±1D y 49.3% vs 46.3% en ± 0.25 D. Aunque en todas estuvo mejor el grupo de FLACS, no hubo diferencias significativas con el odds ratio El porcentaje que alcanzó 20/20 o mejor, 20/25 o mejor y 20/30 0 mejor no tuvieron diferencias estadísticamente significativas62.
En un estudio de Hatch y col 63 se concluye que el láser de Femtosegundo reduce el tiempo efectivo de Facoemulsificación en comparación con la cirugía de catarata estándar en cataratas avanzadas, como se muestra en el siguiente gráfico en donde se observa la reducción del EPT en ambos grupos de núcleos 3 y 5 (NO3 y NO5) de Femto (LCS) donde el EPT es significativamente menor que en los grupos de cirugía con facoemulsificación estándar. Lo que aporta este trabajo es que el Femto puede reducir la necesidad de ultrasonido lo cual no incide en cuanto a la emetropía, pero sí en la posibilidad de tener complicaciones como sufrimiento endotelial que lleve a una queratopatía bullosa.
Su principal ventaja, es la construcción de una rexis circular y perfectamente centrada.
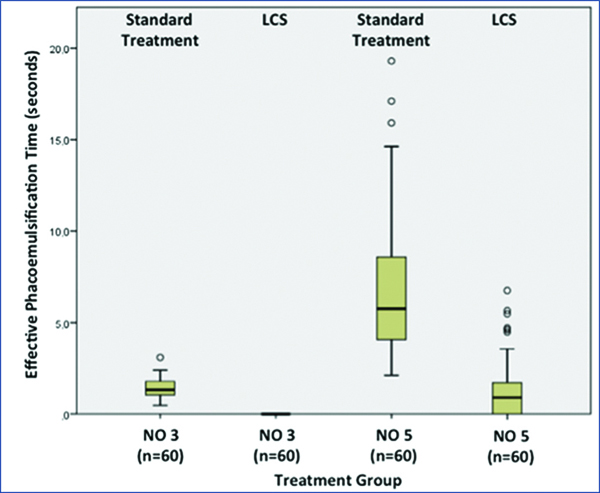
Comparacion del EPT en FLACS y Faco estándar en cataratas Avanzadas.
LIO Panoptix.
Existe un criterio, erróneo, que el centrado de la rexis garantiza un centrado perfecto de la lente.
El centado de la rexis no nos asegura ese centrado, ya que la lente se va a centrar dentro del bag que, como sabemos, no es regular y no es equidistante el centro corneal o el eje visual con las dimensiones del ecuador del cristalino.
Este hecho ha generado que Samuel Masket y Jack Holladay desarrollaran algunos lentes intraoculares que tienen otro criterio de centrado, con la rexis. Estos nuevos lentes se centran en el plano de la rexis, con las hápticas dentro del bag y la óptica, que tiene un surco en el borde donde se encastra la capsulorrexis de la misma manera que una cubierta de bicicleta se encastra en la llanta de la rueda.
Capsulotomìa realizada con laser de femtosegundo ldvz8
El modelo de Masket (Morcher 90S) fue diseñado, en realidad, para intentar evitar las disfotopsias negativas y el Oculentis Femtis fue el diseñado por Holladay como un Femto IOL. Todavía no existen evidencias sobre las ventajas de estos lentes en cuanto al centrado. Se especula que la ubicación del LIO en el plano de la capsulorrexis garantizaría una posición efectiva del lente muy exacta y con esto una consiguiente exactitud mayor en los resultados refractivos.
No obstante, a pesar de estas ventajas todavía no existe una aceptación masiva a la utilización del Femto. Por el contrario, son mayores las críticas. Algunos estudios demuestran que existe un riesgo mayor de ruptura de la cápsula anterior, estadísticamente significativa (P=0.00002) en las capsulorrexis con Femto, 1.87%, comparado con la CCC manual, 0.12%36.


Lentes intraoculares diseñados para cirugia de catarata con láser de femtosegundo.
La segunda ventaja de la CICAFE es la de tener desde el comienzo un núcleo ya fragmentado, este paso reduce la necesidad de ultrasonido, pero no tiene incidencia en la emetropía resultante.
En las otras dos aplicaciones: la realización de la incisión corneal principal y las incisiones corneales para corregir el astigmatismo corneal no existe todavía consenso en cuanto a que signifique o no una ventaja en la búsqueda de la emetropía. Cerca de la mitad de los usuarios de Femto no utilizan las incisiones corneales y dos tercios no usan las de astigmatismo.
Muchos creen que el Femto realiza los pasos de la catarata con una precisión cien veces mayor que con la mano (Carlos Ferroni), otros que no le agrega nada importante.
En el mercado existen varios equipos como el LensX de Alcon, LDV Z8 de Ziemmer; el Victus de Bausch & Lomb; el Catalys de Optimedica; y el LensAR de LensAR. Probablemente el primero sea el más utilizado, afirman en su página haber realizado más de 400.000 procedimientos.
El más móvil y versátil es el LDVZ8 que es fácilmente transportable, tiene módulo de catarata y córnea con el mismo handpiece, pero con diferente descartable que permite trabajar con interfase liquida sin aplanación en Femtofaco y con aplanación para córnea.
La cirugía refractiva en el cristalino es una alternativa que va ganando espacio año a año. Es difícil hacer pronósticos, establecer un probable futuro sobre cuál va a ser la técnica de las décadas venideras. Así como en los 50, un genio como Barraquer apuntaba a la cirugía corneal y pensaba que los comienzos de Ridley eran desalentadores, podemos equivocarnos en esta época de desarrollos vertiginosos de la ciencia.


Láser de femtosegundo ldvz8 (ziemer)
El deseo generalizado de una vida independiente de anteojos nos conduce a la tentación de utilizar la cirugía facorrefractiva cada vez más.
Colocar un multifocal en un hipermétrope ya présbita es aceptable, pero ¿a qué edad es razonable?
¿Es aceptable hacerlo en un miope joven présbita?
Desde ya la cirugía corneal con excímer y de lentes fáquicos es la indicación razonable en los jóvenes no présbitas hasta ahora, pero ¿qué pasará con el desarrollo de los lentes fáquicos multifocales?
El futuro cercano nos va a demostrar la respuesta a algunas de estas preguntas.
LENTES INTRAOCULARES FÁQUICOS
Los lentes intraoculares fáquicos, son aquellos implantes que se colocan sin extraer el cristalino. De acuerdo con su ubicación, se dividen entre lentes de cámara anterior y de cámara posterior.
Lentes fáquicos de cámara anterior
Fueron los primeros en utilizarse, se dividen en lentes de soporte angular y de soporte iridiano. Los de soporte angular fueron los primeros en utilizarse pues se desarrollaron a partir del diseño del modelo Kelman de 4 puntos de fijación, utilizado en la corrección de la afaquia cuando no existía sostén capsular. A partir de este diseño George Baikoff diseñó una lente para corregir la miopía, el ZB5M de Domilens, fabricado en PMMA, que obtenía buenos resultados ópticos a la hora de corregir la miopía, pero con un alto índice de complicaciones, debidas a diferencias en el tamaño del LIO que, si era chico permitía rotar y mover el lente y podía descompensar la córnea, mientras que, si quedaba muy ajustado podía ovalizar y deformar la pupila de modo irreversible, generando a veces lesiones importantes del iris. Otra complicación frecuente era la visualización de halos, pues la pupila en la oscuridad superaba a la óptica. También se describieron casos de síndrome de Urrets Zavalia. Este lente sufrió varias modificaciones en su diseño, que no alcanzaron para disminuir las complicaciones.
A fines de la década del 70, Jan Worst, en Holanda, creó una lente intraocular de soporte iridiano, que tenía por función corregir la afaquia, el Artisan, fabricado todo de PMMA. Originalmente lo quiso llamar Worst Lens, pero dado la connotación negativa que podía tener en el mundo, por la significación de su apellido en inglés (“el peor lente”), lo llamó Iris Claw, que significa “garra” y es el mecanismo por el cual de fija al iris.
En ojos afáquicos los resultaron fueron muy buenos, debido a su éxito en 1986 se implantó en ojos fáquicos, miopes y en 1992 en hipermétropes. En 2004 el Artisan fue aprobado por la FDA. En 2003 se creó el lente Iris Claw plegable (Artiflex), que permitió implantarlo por incisiones pequeñas. Esto habilitó la aparición en 2006 del Iris Claw tórico.
Una de las ventajas del Iris Claw es la reversibilidad, la otra es que “one size fits all” es decir que no existen los problemas de la medición del tamaño de la lente como ocurre en los lentes fáquicos de soporte angular y de cámara posterior.
La posibilidad de desinsertarse, espontáneamente o ante mínimos traumas, existe y los daños sobre el iris también. Si se cumplen las indicaciones, y se tienen en cuenta las dimensiones mínimas de profundidad de la cámara anterior, el riesgo de descompensación corneal es bajo. En USA se llamaron Verysize y Veryflex, ya que Ophthech fue comprada por la firma AMO.
El concepto de este lente es la de soportarse en el iris gracias a la presencia de dos hápticas que atrapan el iris. El cálculo del poder del LIO fáquico Iris Claw es muy exacto con la fórmula de Van der Hejden.
En los casos de afaquia se puede colocar retroiridiano o en cámara anterior, lo importante es tener en cuenta la constante A, que es 115.0 ultrasónica y 115.7 óptica para la ubicación prepupilar y, 116.8 ultrasónica y 116.9 óptica para implantarlo retropupilar.
El lente fáquico de cámara posterior ICL (Staar Collamer Implantable Contact Lens) ha ido desarrollándose desde hace más de 20 años, a través de varios modelos que han sido modificados en algunos detalles de diseño menores. En el nuevo modelo se introdujo una modificación muy importante, diría que paradigmática, como la del modelo V4c que incorporó un orificio central, de 0.36 mm de diámetro, el KS aquaport, que tiene por fundamento mejorar la circulación del humor acuoso, reduce la probabilidad de la formación de catarata y evitar la necesidad de realizar iridotomías periféricas, que debían realizarse con el objeto de que no se produjera el bloqueo pupilar.
Uno de los principales problemas que se plantearon desde el comienzo de la utilización del ICL, fue el tema del vaulting (distancia entre el cristalino central y el lente) que no debía ser demasiado grande (generalmente el límite se considera 1000 micras), que genere un problema de cierre angular ni demasiado poco, que contacte el lente con el cristalino, y pueda provocar catarata (150 micras se consideran como el mínimo, por debajo entramos en la zona de riesgo). El vaulting es una función del tamaño del lente, cuyo diámetro se elige de acuerdo con la medida del White to White horizontal. Algunos casos han demostrado que la medida horizontal del sulcus to sulcus no siempre se correlaciona con el W to W. Existen numerosas maneras de realizar esta medición, con compás o caliper, con el Orbscan, con el Pentacam, el Lenstar, el del IOLMaster, algunos son más exactos y otros menos, cada cirujano confía más en uno u otro equipo.
Algunos estudios proponen realizar de rutina el UBM preoperatorio, con la medición del sulcus to sulcus horizontal, para descartar variantes anatómicas individuales que pueden generar mal posicionamiento del lente, aunque muchos continúan sosteniendo que debe elegirse el white to white para calcularlo.
Actualmente con diferentes tecnologías que permiten visualizar el surco iridociliar, como el UBM, reducimos algunos problemas relacionados con la presencia de quistes iridociliares que pueden dificultar o aún impedir la colocación correcta del ICL.
Los primeros estudios sobre los resultados publicados de implante de ICL, en 1998 por Roberto Zaldivar en el Journal of Refractive Surgery sobre la corrección de la miopía31 e hipermetropía32 muestran la eficacia, estabilidad y seguridad. En los miopes, cerca de un 36% ganaba 2 o más líneas de AV y más de un 45% quedaba con un error refractivo de ± 0.50D y, en los hipermétropes 58% en ± 0.50, y sólo el 8% ganando más de 2 líneas. En esta época se recomendaba enfáticamente la realización de iridotomías patentes, sobre todo en los hipermétropes, mientras hoy con el Aquaport no es necesario. Los resultados actuales muestran una mayor exactitud en los cálculos del poder del lente con un 87% en ± 0.5 D.
El Bioptics35, publicado por primera vez por Roberto Zaldivar, que corresponde a la combinación de LIO fáquico con LASIK posterior, en casos de miopías elevadas cuando el lente fáquico no alcanza a corregir el defecto refractivo, permitió aumentar el rango de corrección de las miopías y corregir los errores post quirúrgicos en pseudofáquicos.
En un trabajo que compara el implante de un ICL en un ojo y LASIK en el congénere del mismo paciente, Pallikaris33 concluye que mejor calidad de visión, estabilidad, score de satisfacción se obtienen en el ojo del ICL. Existen múltiples trabajos comparativos entre los diferentes modelos de lentes fáquicos, uno compara ICL tórico con Artisan tórico en donde se observa una satisfacción mayor con el Visian34.
En el 2010 comenzó a ser utilizado también para corregir, como piggy back, defectos refractivos pseudofáquicos de miopía, hipermetropía y astigmatismo. En los últimos años existe un modelo de lente fáquico de cámara posterior multifocal, que puede colocarse en ojos fáquicos o pseudofáquicos que todavía no tiene casuística suficiente para evidenciar seguridad y eficacia.
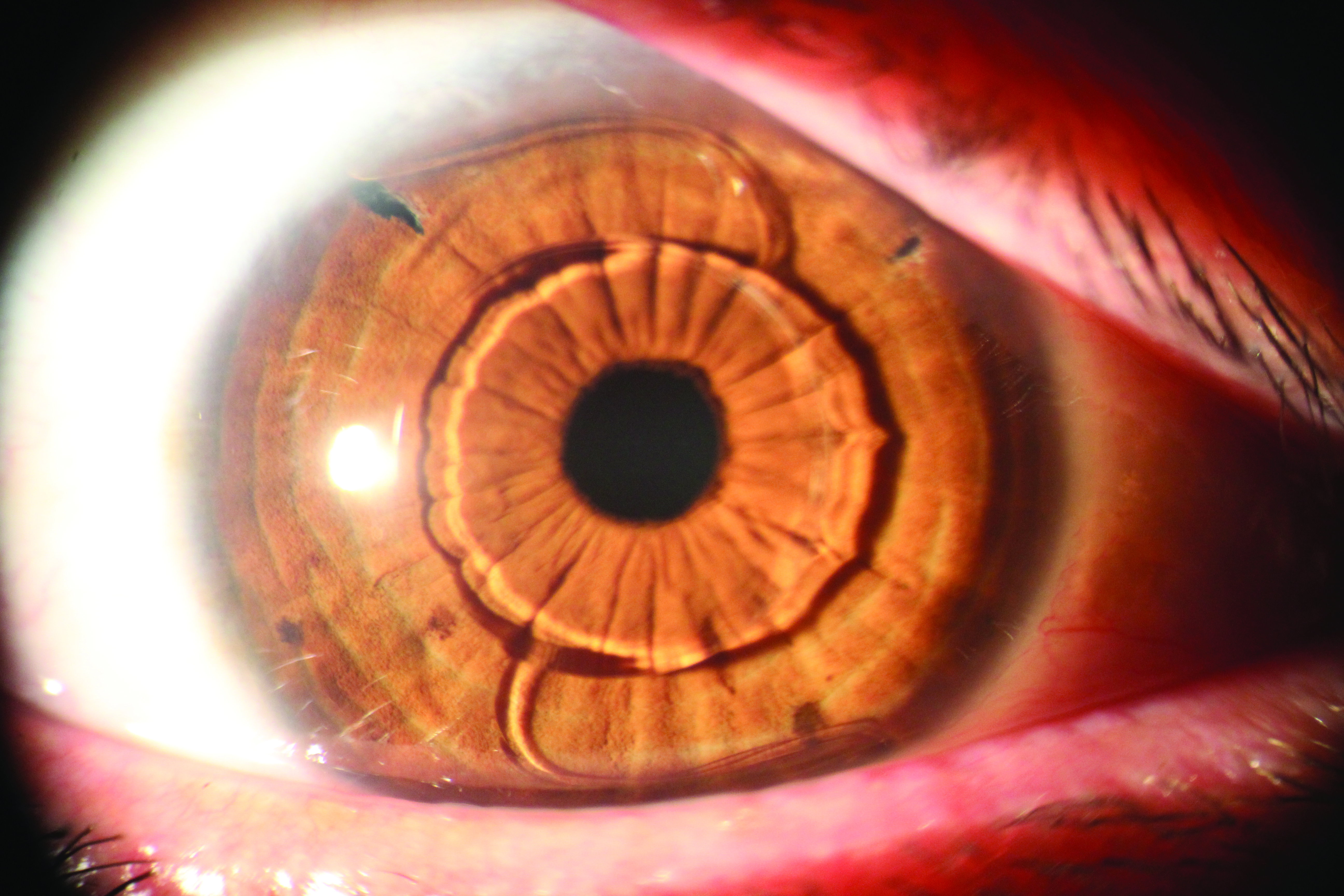
Lente fáquico de cámara anterior Phakic 6.

Lente fáquico de cámara anterior baikoff
con ovalización de pupila.
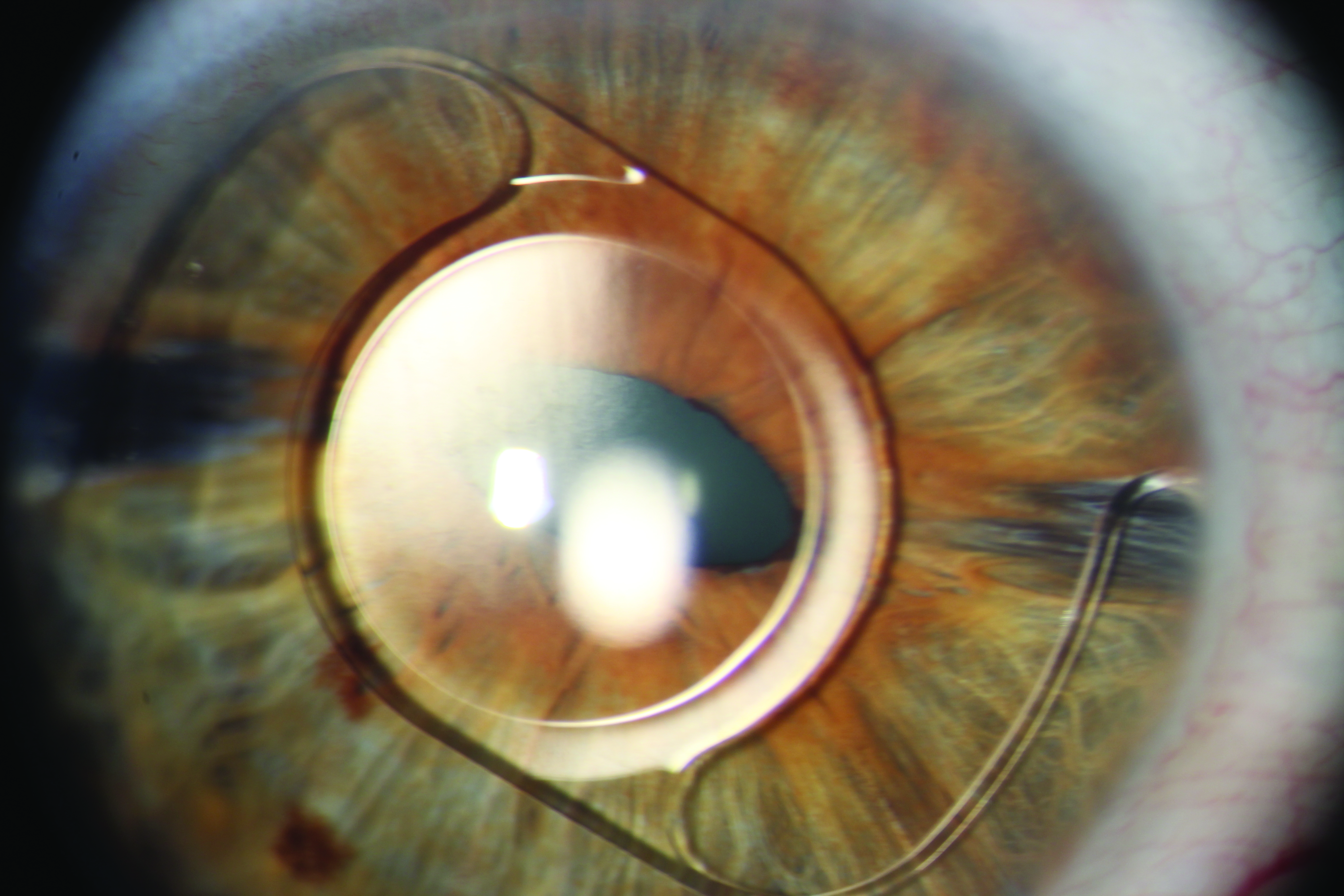
Lio fáquico de cámara con soporte angular y defecto iridiano.
.JPG)
Lente fáquico de cámara anterior con soporte iridiano Artisan.
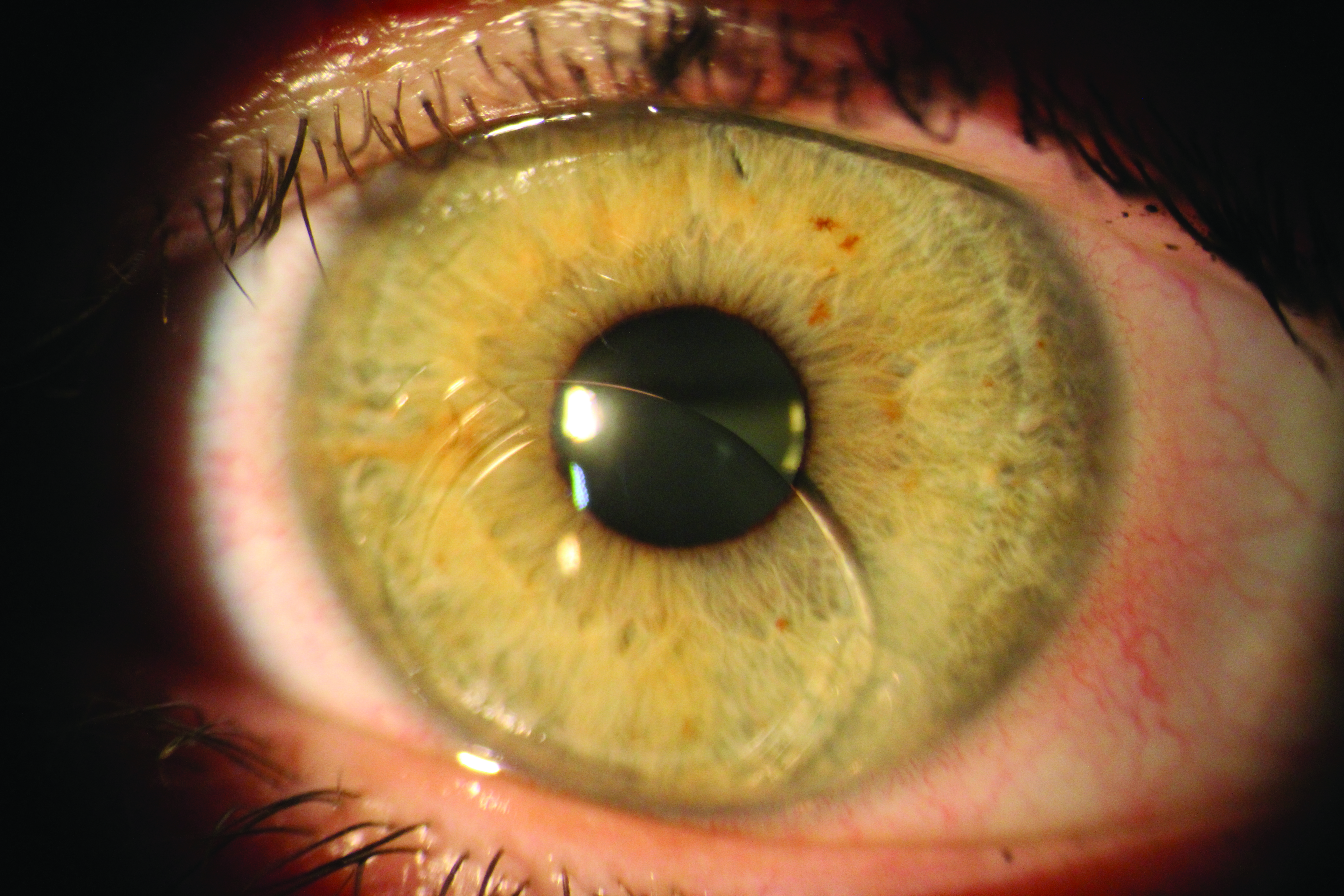
Lente Artiflex dislocado post trauma.
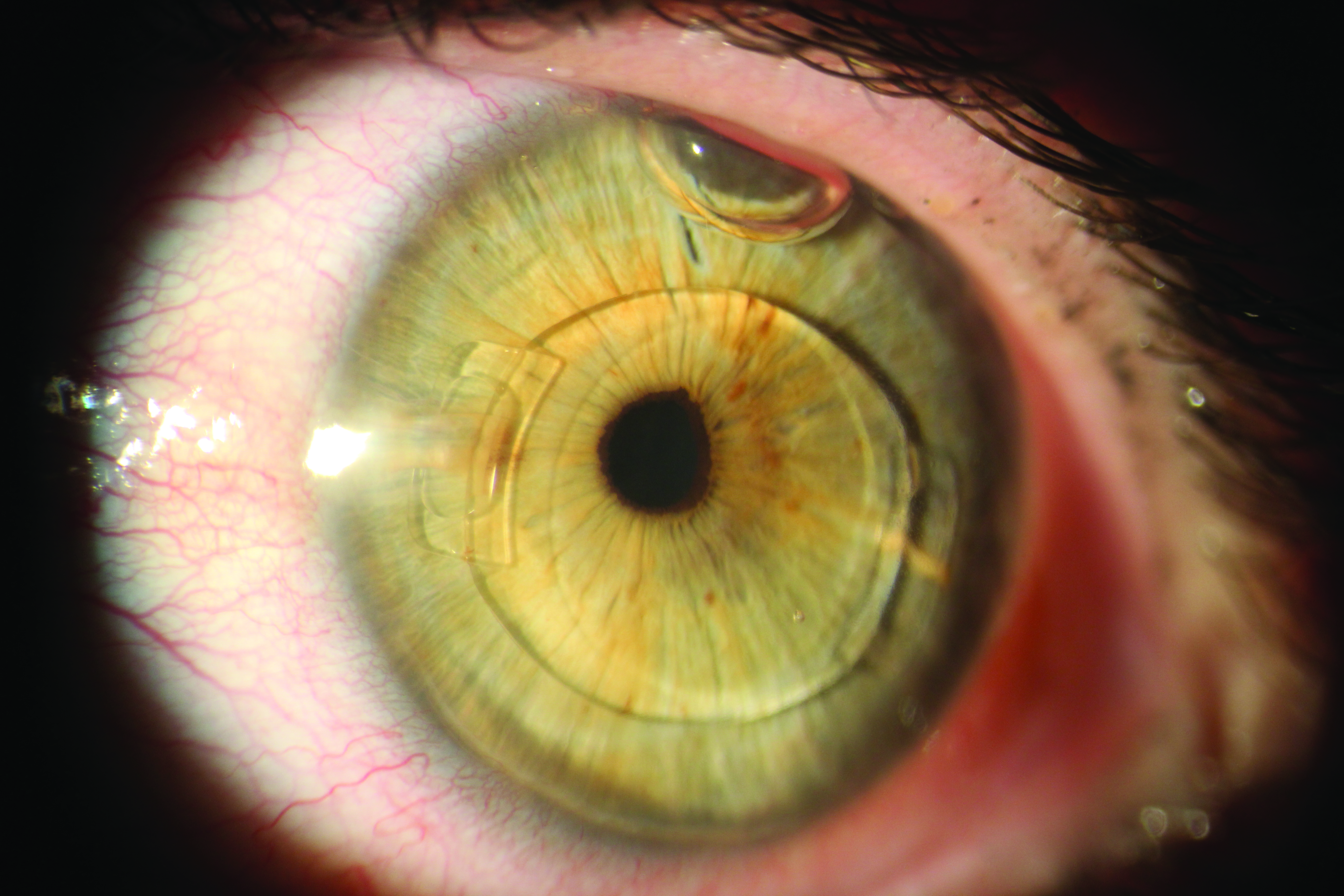
Lente Artiflex reposicionado.
ICL con Aquaport
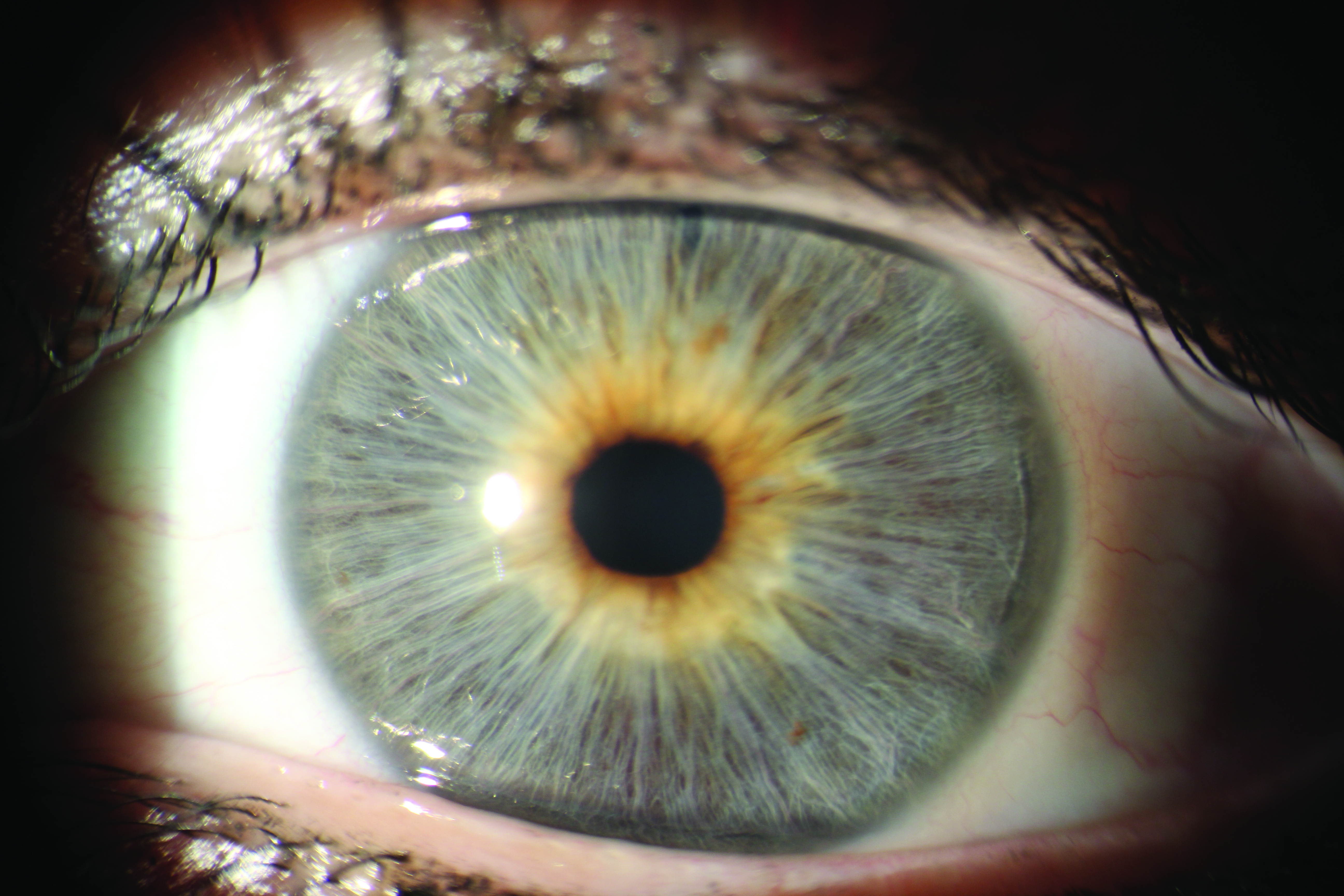
ICL con iridotomía superior.

LIO fáquico de CP.
IMPLANTE SECUNDARIO DE LENTES INTRAOCULARES
Este gran capítulo de la corrección quirúrgica hacia la emetropía incluye todos los procedimientos que se pueden realizar en aquellos ojos que han quedado afáquicos o pseudofáquicos con un defecto refractivo residual.
Aquellos casos que, como consecuencia de traumas, cirugías de retina con extracción de cristalino, luxaciones de complejos lente-saco, no queda sostén capsular y se debe colocar una lente para corregir la afaquia.
Una opción utilizada en los 80 fue la de implantar LIO de cámara anterior. El diseño de éstos fue de Kelman, con 4 puntos de contacto en el ángulo, iridocorneal, todo en PMMA, que requería abrir la incisión más de 6.5 mm y con el inconveniente que debíamos tener un stock de diferentes diámetros que varían según el wtw del paciente. Las complicaciones de estos lentes, descompensación corneal, deformación pupilar y defectos marcados en el iris llevaron a casi su total abandono en la actualidad.
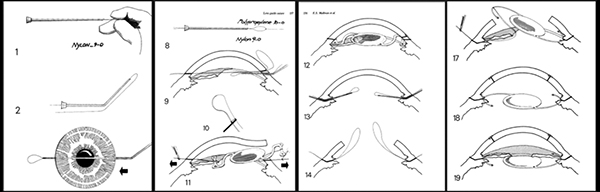
En 1986 Enrique Malbran 51 publica un trabajo en donde propone distintas alternativas para suturar a esclera un lente de cámara posterior, con suturas de nylon 9-0 o polypropilene 10-0 guiadas por agujas, con las consiguientes ventajas sobre los de cámara anterior que eran las únicas que se utilizaban en ese momento. Este trabajo fue capital para modificar el manejo de la corrección de la afaquia, muchas técnicas derivaron de esta publicación. Hoy día continuamente es citado en toda nueva manera de fijar un lente en ausencia de sostén capsular.
En los esquemas siguientes, que son los originales publicados, se ve una aguja enhebrada con una pasada (1 y 2 en el dibujo) y con dos pasadas (8) creando un lazo que toma el háptica de la lente. El procedimiento estaba destinado a la afaquia sin sostén en queratoplastia inclusive (14 a 19).
Otro lente que continúa teniendo su utilidad es el implante del LIO de tipo iris claw Artisan (Ophtec) modelo 205 de afaquia, que puede colocarse en su posición original prepupilar, pero también retropupilar.
El lente es el mismo, mide 5.4 mm de ancho y 8.5 mm de largo, la técnica es similar, con la pinza de sostén del lente y enclavando el iris con el gancho o con el sistema VacuFix.
Recordamos que la única variante es que tenemos que considerar son las distintas constantes para el cálculo prepupilar y retropupilar.
En cuanto a las otras técnicas de fijación de lentes secundarios, existen múltiples formas de hacerlo utilizando lentes de cámara posterior.
En principio, la sutura al iris de un lente de tres piezas, con Prolene 9-0 o 10-0. Esta técnica puede generar casos de síndrome de UGH, sobre todo si el lente tiene borde cuadrado y produce rozamiento con el iris. El cálculo del poder del lente en estos casos debe contemplar que hay que modificar el poder del lente, que generalmente es al bag, y calcularlo al surco. Es muy útil el aporte de Warren Hill, quien en su página web publicó una tabla de conversión Bag-sulcus de todos los poderes y que es una herramienta muy útil para tener en el quirófano. El problema es sobre todo en los poderes mayores a 17.50 D, en los cuales puede haber un shiff miópico de 1 D o más.
Las otras innumerables técnicas de fijación a esclera, con sutura de Prolene o Goretex, tienen sus complicaciones derivadas de la dificultad del manejo de las suturas.
Uno de los problemas surge de la posibilidad que se extruyan los nudos de la sutura y generen molestias, el riesgo de infección y el corte de la sutura por alguien que lo ve extruido y no piensa que ese punto está sosteniendo el LIO.
Hay muchas variantes para ocultarlo y quede bien oculto, como la de crear una tapa escleral, un surco de una profundidad de la mitad del espesor escleral, horizontales o verticales, y luego enterrar el nudo, y actualmente el bolsillo de Hoffman, que es un bolsillo invertido desde la córnea hacia afuera a 400 μ de profundidad donde queda alojado el nudo. Uno de los problemas de las suturas horizontales es la posibilidad que provoquen un tilt del lente. Estas técnicas generalmente se utilizan para reposicionar un lente o complejo lente saco luxados, conservando el LIO original.
Cuando se debe implantar un lente secundario en ausencia de sostén capsular, la técnica que actualmente se ha transformado en la preferida es la de Yamane, que es una modificación de la de Agarwal, en las cuales se fijan las hápticas de prolene en la esclera sin mediar suturas. Estas se colocan aproximadamente a 2 mm del limbo que equivaldría al poder del lente colocado en el bag.
La técnica de Agarwal crea unas tapas esclerales con un surco lateral a la escotilla tallado en la esclera, se extrae el háptica con micropinzas, se enhebra en ese túnel paralelo al limbo el extremo del háptica y luego se cierra con adhesivos tisulares.
En la de Yamane se enhebran las hápticas del LIO de 3 piezas con unas agujas que tallan un canal paralelo al limbo y se extraen los extremos de las hápticas a través de la aguja, cauterizando suavemente los extremos para crear un freno que impida que se deslice el háptica hacia el interior del ojo.
En estas dos técnicas el tilt es menos probable, y con ello la probabilidad de crear astigmatismo por la inclinación de la lente.
Todas estas técnicas de fijación, aunque estén bien posicionados los lentes, generan una posición efectiva incierta, hay que tener en cuenta la variabilidad que puede existir, por lo cual la refracción final es imprecisa.

LIO Sulcoflex
Existen como vimos modelos de LIO diseñados especialmente para ser colocados en el surco, fabricados por la firma Rayner, el modelo Sulcoflex, para errores post pseudofaquia, que incluye defectos esféricos y cilíndricos.
No se colocan en ausencia de soporte, siempre sobre otro lente implantado previamente.

HD Analyzer
CALIDAD VISUAL
Hasta aquí hemos presentado las tecnologías relacionadas con obtener emetropía, libres de defectos o vicios de refracción. En los últimos años comenzó a difundirse un concepto que es más abarcador que la refracción objetiva y que se conoce como calidad visual. Este concepto está basado en considerar que 20/20 no es suficiente para definir una buena visión, es decir, que podemos llegar a ver los optotipos de Snellen de la fila de 20/20, pero eso no significa una buena resolución de esa imagen.
El tema es que el complejo proceso de la percepción de las imágenes comprende elementos ópticos y componentes neurológicos de cómo esa imagen proyectada en la retina es procesada a nivel de la vía óptica.
En cuanto a lo que comprende a la formación de la imagen que es percibida en la retina, en los últimos años se ha desarrollado una tecnología que intenta estudiar el sistema óptico visual como usualmente se explora cualquier sistema óptico, como un telescopio, un lente intraocular o una lente fotográfica, tratando de proveer una medida objetiva de la calidad de ese sistema óptico como lente.
El HD Analyzer es una herramienta que puede medir la dispersión que sufre un haz luminoso al atravesar el sistema óptico ocular cuantitativamente. Esta capacidad es particularmente importante en algunas situaciones: diagnóstico en cataratas precoces, ojo seco en pacientes asintomáticos y para seleccionar procedimientos refractivos más adecuados a cada caso. El estudio se realiza a través de un doble paso de un haz infrarrojo de 2 mm de diámetro, que produce una imagen en la retina circular, y del análisis de la dispersión de esa imagen puntual (PSF). A partir de esa imagen capturada y la evaluación de esa dispersión, surge un índice de dispersión objetiva (OSI). Previamente realiza una medida de la refracción objetiva que permite calibrar el sistema para eliminar la dispersión provocada por el error refractivo. Cuando el OSI es menor que 1 (en la gama de los verdes) no existe dispersión significativa, si es en amarillo es que hay una catarata que está provocando una mayor dispersión y, en rojo, ya se trata de una catarata más importante.
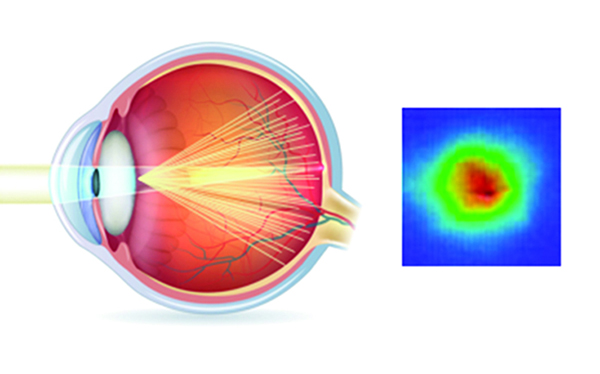
Midiendo la calidad visual tenemos tres valores: el PSF (Point spred function) que es la distribución espacial de la luz que, en el plano de la imagen, genera una luz puntual; el MTF (Modular transfer factor) que es el grado de nitidez, la sensibilidad de contraste luego de pasar a través de un sistema óptico y el OSI (Objetive scatter index) que analizamos antes y da un índice de la dispersión objetiva.
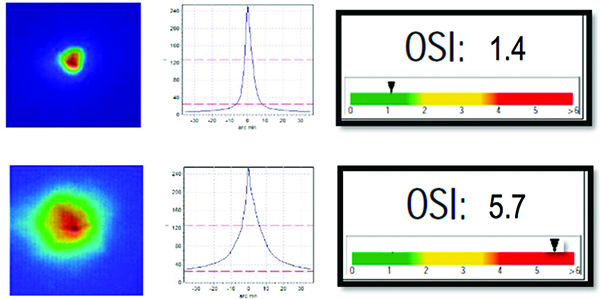
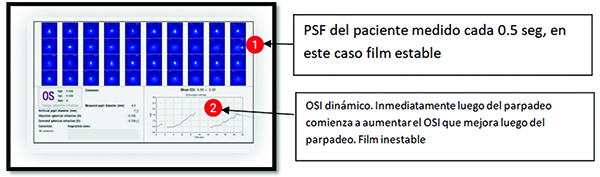
Otra de las ventajas que brinda esta tecnología es la posibilidad de tener una idea objetiva de la estabilidad de la película lagrimal. A través de una medición dinámica (cada 0.5 seg) del OSI, puede evaluar pacientes con síndrome de ojo seco, en el preoperatorio de una cirugía refractiva o facorefractiva, y comprobar que mejora con el tratamiento o no, para evitar poner un lente multifocal o indicar un lasik. Las curvas del OSI clasifican en 4 grupos: I normal, II y III anormales que pueden mejorar con tratamiento y IV que incluye a los casos severos, en los que no conviene realizar procedimientos con LIO premium, como fue estudiado por Roger Zaldivar.
TOPOGRAFÍA CORNEAL
A medida que la cirugía refractiva fue evolucionando desde la cirugía incisional, fue tornándose imprescindible tener un conocimiento sobre el contorno de la córnea, más allá de la queratometría, dado que la córnea es asférica, asimétrica e irregular.
Esta necesidad dio lugar a nuevas tecnologías, cuya denominación genérica incluye el término de topografía corneal.
Probablemente el término no sea el más apropiado, pero es el que se impuso.
La manera en que estos equipos miden la curvatura es variable: por un lado, están los sistemas basados en el disco de Placido. Este disco está constituido por anillos analizadores que se proyectan sobre la cara anterior de la córnea y se analiza la imagen reflejada, cuán cerca o más alejados están entre sí estos anillos, midiendo el ángulo de reflexión, podemos evaluar la pendiente y analizar la curva de esa córnea.
Otros equipos analizan la elevación, utilizando una grilla de proyección, y presentando los mapas de elevación de la superficie de cara anterior y posterior de la córnea.
Los primeros topógrafos en realidad hacían una videoqueratoscopia, a partir de un disco de Placido, utilizaban la proyección de una imagen de círculos concéntricos en la cara anterior de la córnea que, combinando la imagen de video digital y el análisis computarizado, le adicionaba el carácter cuantitativo (Klyce 1987) imprescindible para evaluar la córnea.
En ese mismo año se publicó el primer mapa cuantitativo codificado con colores. Estos equipos tienen la capacidad de analizar miles de puntos en pocos segundos y construir mapas codificados. El mapa más utilizado es el axial (sagital). Los algoritmos utilizados son en base a la comparación con la geometría de una esfera. Este es el más útil para evaluar astigmatismos regulares y detectar irregularidades, pero no para detectar aberraciones.
Esta limitación del sesgo esférico, y la necesidad de intentar conocer la forma real de la córnea asférica, lleva a otro tipo de topógrafos que utilizan algoritmos más complejos, con mapas tangenciales o de curvatura instantánea.
Estos avances en otro tipo de algoritmo, da origen a la topografía de elevación. La forma verdadera de la córnea depende de la medición en un sistema de coordenadas X, Y y Z.
En 1995 se introduce el Orbscan (Bausch & Lomb) que utilizaba cortes seccionales ópticos para medir la elevación, a través de una hendidura de barrido que podía evaluar la curvatura y elevación de la cara anterior y posterior de la córnea. Sin embargo, la generación de los datos de elevación del Orbscan depende adicionalmente de una videoqueratoscopía estándar de Placido ya que este método tiene cierta limitación para medir la elevación en forma precisa.
Topógrafo ORBSCAN (Bausch & Lomb).
El topógrafo que puede considerarse de elevación puro es el Pentacam (Oculus) que utiliza el principio de Scheimpflug. Esta técnica se cree que es más precisa para medir que una cámara coaxial. En el Pentacam la cámara rota 180° alrededor de un punto, mientras el paciente fija una luz central. Una segunda cámara detecta cambios de posición y el software corrige el resultado. La computadora analiza 2760 puntos de datos para cada imagen obtenida.
La otra tecnología que ha contribuido a mejorar los resultados de la cirugía refractiva moderna es la aberrometría.
El concepto básico que es necesario para entender qué es una aberración (aberratio, del latin salirse del camino) es el de “frente de onda”. La luz es una onda electromagnética, con un movimiento oscilatorio que se propaga. La superficie en la que todos los puntos de un medio son alcanzados por la onda al mismo tiempo es el frente de onda. Una alteración en el frente de onda al atravesar un medio óptico es una aberración. En condiciones ideales, si no hubiera aberraciones, en un frente de onda que atraviesa un medio óptico de un ojo emétrope, sigue su camino con los rayos de luz en fase, mientras que, si existen aberraciones y no convergen adecuadamente, algunos desviarán su camino y hablaremos de un frente de onda aberrado.
La representación de las aberraciones se representa en un mapa bidimensional de colores.
Se puede calcular el PSF y el MTF de un medio óptico.
También puede representarse la forma del frente de onda por los polinomios de Zernike, introducidos en 1934 y que se obtienen a través de una función matemática muy compleja. Representados en coordenadas cartesianas x,y,z, o polares (ρ, Θ).
La calidad óptica de la imagen retiniana se determina por las aberraciones oculares, la difracción y la dispersión intraocular.
Las aberraciones oculares se clasifican en aberraciones monocromáticas y cromáticas. A su vez, las primeras pueden ser divididas en aberraciones de bajo orden (que incluyen los errores refractivos) y de alto orden, que no pueden corregirse con lentes como las de bajo orden.
El sistema óptico ocular presenta gran variedad de aberraciones, debido a que el eje visual no coincide con el eje óptico y a que las superficies ópticas son asimétricas.
En la pirámide tenemos representadas las aberraciones, cuanto más arriba de la pirámide y más central al eje, mayor es el impacto en la calidad visual del paciente, mientras que, es menor cuanto más alejada del eje y más abajo se encuentra. La gama del verde se representa un nivel cero de medida en micras, es decir, ningún error aberrométrico, los colores fríos representan el frente de onda lento, atrasado o retardado en micras con respecto al plano ideal, mientras que los colores cálidos representan un frente de onda avanzado respecto al frente de onda ideal. En cada fila están ubicadas las del mismo orden. Toda la información del frente de onda se puede resumir en un solo número, como error cuadrático medio o RMS, que es un compendio de los coeficientes de Zernike y brinda una estimación de la diferencia con el frente de onda ideal en micras.
Cuanto menor es el valor de RMS, mejor es el frente de onda real y más óptima la calidad visual del paciente y estimación de la agudeza visual (RMS=1, AV 20/20; RMS=1.5, AV 20/80).
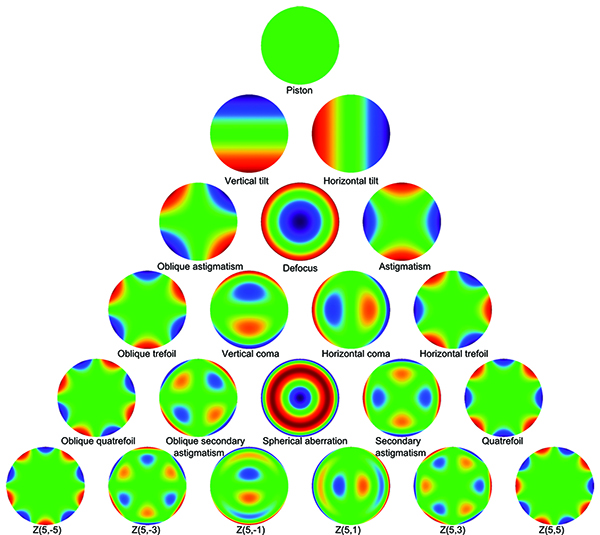
Las aberraciones de bajo orden (o de segundo orden) se conocen como errores refractivos esférico y cilíndrico (desenfoque y astigmatismo).
Las aberraciones de alto orden (HOA) son las que se encuentran a partir del tercer orden y no tienen corrección óptica, aunque a través de la introducción de la ablación personalizada del frente de onda, es posible su corrección.
El estudio de la topografía y las aberraciones de la córnea y del cristalino se hace cada vez más necesario, por el uso creciente de los lentes intraoculares premium que obligan a un acercamiento más personalizado en los estudios preoperatorios, sabiendo discernir cuales detalles son importantes a la hora de decidir en qué ojos no implantar un lente multifocal. En la época en que los lentes eran solamente esféricos, donde la satisfacción del paciente dependía del poder del lente. Depende del poder del lente, pero hoy día hay que evaluar expectativas, hobbies y las características del tipo de ojo, sus aberraciones, etc.
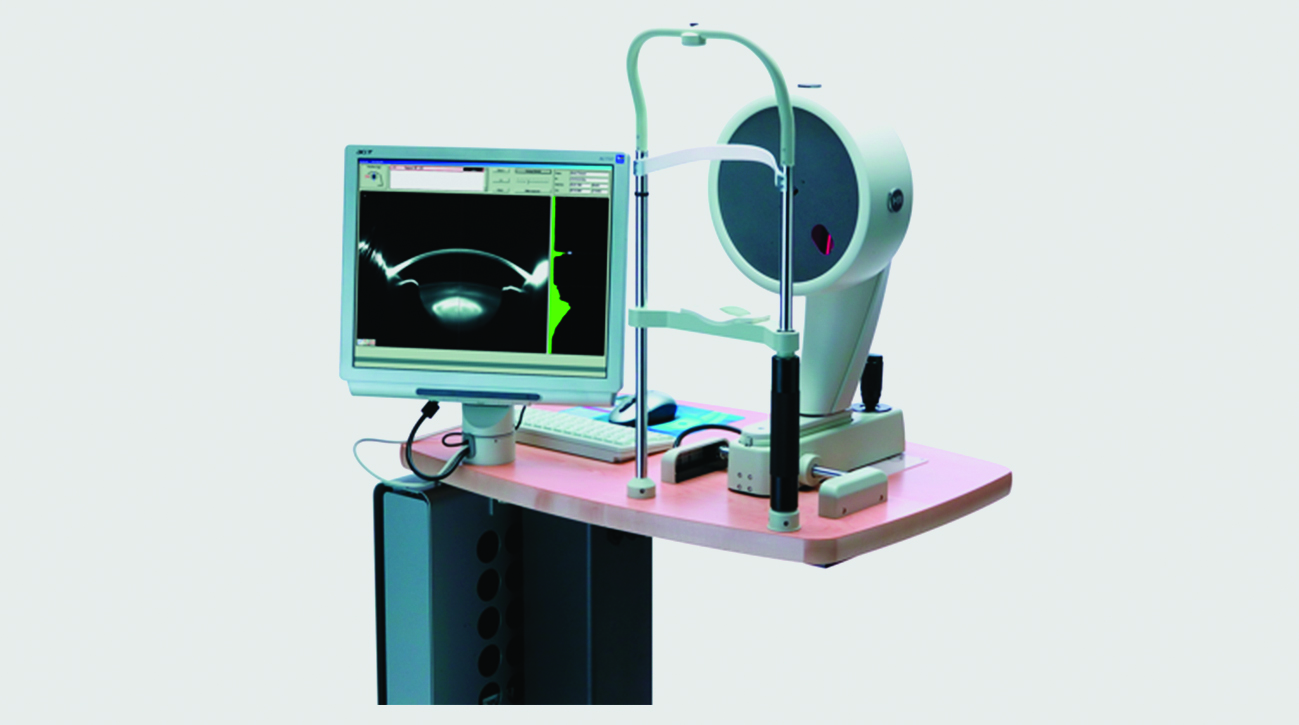
Pentacam (Oculus).
En este sentido los equipos que disponemos, como el Pentacam (Oculus) o el OPD III (Nidek) aportan muchos detalles a los que debemos prestar atención en el preoperatorio de la facoemulsificación premium.
En el manual del Pentacam recomiendan evaluar el análisis corneal tomográfico (Scheimflug) especialmente: el poder refractivo corneal total, el astigmatismo corneal irregular (aberraciones de alto orden), las aberraciones esféricas corneales y el cilindro corneal. Además, observar la K simulada, la ACD, el diámetro pupilar, espesor corneal.
Cuando las aberraciones totales de alto orden (HOA) son 0.180 μm, las aberraciones esféricas (SA) de 0.307 μm, la relación front-back (80.5%) y el cilindro (-0.5 D), estamos en rango normal. En estos casos se pueden implantar asférico multifocal o monofocal de acuerdo con la calidad de la córnea, aún en cámara estrecha.
Por el contrario, si en un post LASIK, las HOA son 1.575 μm, altas y las SA -1.355 μm, muy bajas, convendría colocar un LIO esférico con reservas por la irregularidad corneal que puede impactar en la calidad visual.
Si las HOA son 0.360 μm, que muestran un leve astigmatismo irregular y las SA en 0.403 μm, relativamente alto en límite normal. Podría usarse un asférico monofocal usando las fórmulas para post LASIK.En la medida que operamos cataratas más incipientes, es muy importante evaluar detalles de los mapas tomográficos para no pasar por alto astigmatismos irregulares leves que comprometan la calidad visual post operatoria. El límite de las HOA a 4 mm es de 0.3μ para astigmatismos irregulares leves y 0.5μ para los moderados. En los operados previamente de Lasik, hay que analizar muy bien la forma de la córnea y detectar irregularidades que puedan generar errores en el LIO. Evaluar las SA que no siempre se ajustan a la regla de lo esperado en el post LASIK miópico e hipermetrópico. Los lentes asféricas deberían ser implantadas cuando las aberraciones estén en 0.1 μ o más. Algunos lentes tóricos pueden ser implantados en ojos con astigmatismos irregulares leves, pero deben analizarse las HOA y con frente de onda, no con queratometría, el eje del astigmatismo.
La cantidad de información que brindan estos equipos puede ser un auxiliar invalorable para la práctica de la cirugía refractiva actual.
Otro elemento importante es el ángulo Kappa, que es el ángulo entre el eje visual y el eje de la pupila. Clínicamente, es importante para el cirujano refractivo porque los pacientes, especialmente los hipermétropes, tienen un ángulo kappa grande, que hace que el centro de la pupila no coincida con el punto por el que pasa un rayo de luz centrado en la fóvea. Un tratamiento que considera el centro de la pupila, producirá una ablación descentrada si no se compensa con el ángulo kappa, las aberraciones de alto orden empeoran.
En los LIOs multifocales adquiere un mayor relieve, si el ángulo kappa es muy grande, y el anillo central del MIOL es muy pequeño, el eje de la fijación puede pasar no por el centro de la lente sino por el borde del primer anillo. La diferencia de un 0.5 sería hoy dia la aceptada como límite para colocar este tipo de lentes intraoculares.
CONCLUSIONES
La conjunción de una técnica depurada, microincisiones que no inducen prácticamente astigmatismo, topógrafos que permiten entender mejor la problemática del astigmatismo, máquinas confiables para extraer el cristalino, lentes intraoculares monofocales y multifocales que corrigen astigmatismos y el acceso a fórmulas más precisas, calculadores on line, aparatos de medición de última generación con tecnología Swept source OCT nos llevó a que la cirugía facorrefractiva sea una realidad.
El excimer laser con ablaciones muy regulares, controladas por topógrafos y aberrómetros que condujeron a poder saber con seguridad qué casos son operables y cuáles no son buenos candidatos para ofrecer técnicas de ablación, cuándo hacer LASIK o superficie con seguridad y sin el riesgo de las ectasias tan temibles y frecuentes hace décadas.
Cuando no se puede hacer cirugía corneal y está indicado colocar un lente fáquico, poder brindar la posibilidad de corregir un miope joven con intolerancia al lente de contacto; en estos casos aprendimos que los lentes fáquicos de soporte angular no funcionan, generan descompensación corneal, ovalización pupilar y lesiones iridianas irreversibles, el último intento fue el Caché que fue sacado del mercado en 2011. En este punto, el futuro dará su veredicto, persisten los iris claw y los de cámara posterior.
La balanza, en cuanto a la preferencia de los cirujanos en el mundo, se inclina hacia el ICL que con el invento del Aquaport y los métodos de examen del surco irido-ciliar se evitan dos grandes potenciales problemas, el glaucoma por bloqueo pupilar y la catarata por retención del viscoelástico.
Muchos procedimientos han sido completamente abandonados, la queratotomía radial, epiqueratofaquia, la termoqueratoplastia, la cirugía escleral para la presbicia, los lentes intraoculares acomodativos, la ALK, etc.
Algunas técnicas han regresado bajo otro formato, por ejemplo, el SMILE es una derivación del Flex que proviene de la Keratomileusis lamelar automatizada, utilizando el concepto de la incisión pequeña evitando la creación de un flap.
Los inlays, gracias al femtosegundo también evitan el flap completo tallando uno sectorial, un pocket.
Hubo errores y técnicas que debieron abandonarse luego de conocerse las complicaciones que producía; modelos de lentes intraoculares que tuvieron su momento de gloria; equipos que consiguieron aprobación de la FDA y después se abandonaron como la Queratoplastia Conductiva; pero hubo precursores que trabajaron muy pacientemente para conseguir perfeccionar un método que al principio fue abrazado por pocos que no comprendían lo que pensó Kelman en 1967.
La historia del conocimiento en todas las áreas de las ciencias de la Humanidad es una sucesión de logros gratificantes, fracasos decepcionantes, pequeños pasos cuya importancia valoramos muchos años después, grandes avances que se advierten como paradigmáticos en el instante.
Mi idea al proponer este Relato Anual fue la de transmitir a las generaciones presentes esta vivencia: donde estamos hoy es el resultado del aporte tesonero, oportuno e imprescindible de quienes han sido pioneros en hacer posible una idea: Ridley, Barraquer, Fiodorov, Sato, Ruiz, Carriazo, Kelman, Worst, Pallikaris, Malbran, Gimbel, Neuham, Shimitsu, Nagahara, Zaldivar, Haigis, Holladay, Barrett, Hill y tantos otros que continuarán aportando en este devenir sin fin.
BIBLIOGRAFÍA
1. Ridley, H Brit.J.Ophthal. 36,113. (1952)
2. Fyodorov SN, Kolinko Al. Estimation of optical power of intraocular lens. Vesin Oftalmol 1967; 80: 27-31.
3. Colenbrander MC. Calculation of the power of an iris clip Iens for distance vision. Br J Ophthalmol 1973; 57: 735-40.
4. Thijssen JM. The emmetropic and the iseiconic implant Iens: computer calculation of the refractive power and its accuracy. Ophthalmologica 1975; 171: 467-86.
5. Van der Heijde GL. A nomogram for calculating the power of the prepupillary lens in the aphakic eye. Bibl Oplithalmol 1975; 83: 273-5.
6. Binkhorst RD. The optical design of intraocular lens implants. Ophthalmic Surg 1975; 6: 17-31.
7. Retzlaff J. Sanders D, Kraff M. A manual of implant power calculation. Oregon: Medford, 1982.
8. Retzlaff J. A new intraocular lens calculation formula. Am intraOcular lmplant Soc J 1980; 6: 148-52.
9. Sanders D, Kraff M. Improvement of intraocular lens power calculation using empirical data. Am Intra-Ocular lmplant Soc J 1980;6: 148-52.
10. Retzlaff J. Posterior chamber implant power calculation: regression formulas. Am Intra-Ocular lmplant Soc J 1980; 6: 268-70.
11. Sanders D, Retzlaff J, Krakff M, et al. Comparison of accuracy of Binkhorst, Colenbrander and SRK implant power prediction formulas. Am Intra-Ocular lmplant Soc J 1981; 7: 337-40.
12. Menezo JL, Chaques V, Harto M. The SRK regression formula in calculating the dioptric power of intraocular lenses. British Journal of Ophthalmology, 1984, 68, 235-237.
13. Koch DD. Corneal optics for IOL selection: Cracking the code. Paper presented at: the ASCRS annual meeting; April 20-24, 2012; Chicago.
14. Abulafia A, Barrett GD, Kleinmann G, et al. Prediction of refractive outcome with toric intraocular lens implants. J Cataract Refract Surg. 2015 May;41(5):936-44.
15. Koch DD, Jenkins RB, Weikert MP, et al. Correcting astigmatism with toric intraocular lenses: Effect of posterior corneal astigmatism. J Cataract Refract Surg. 2013; 39:1803-1809.
16. Barrett GD, Abulafia A. Improving outcomes with toric intraocular lenses. Paper presented at: the XXXII Congress of the ESCRS; September 13-17, 2014; London.
17. Barry P. ESCRS/EUREQUO FLACS Study. Paper presented at: the XXXII Congress of the ESCRS. September 13-17, 2014; London.
18. Alio, Jorge y col. Buscando la excelencia en la cirugía de la catarata.
19. Waring GO III, Lyn MJ, McDonnell PJ. Results of the PERK study 10 years after surgery. Arch Ophthalmol. 1994 Oct; 112 (10): 1298-308.
20. Argento CJ, Fernandez Mendy J, Cosentino MJ. J Cataract and Refractive Surg. Laser in situ keratomileusis versus arcuate keratotomy to treat astigmatism. 1999 Mar; 25 (3): 374-82.
21. Barraquer JI. Método para la talla de injertos laminares en córnea congelada; nueva orientación para la cirugía refractiva. Arch. Soc amer oftal. optomo (1958) - 1 – 271
22. Barraquer JI. Arch. Soc amer oftal. optomo (1964) - 5 – 27.
23. Malbran, J., (1954). Una nueva orientación Quirúrgica contra la Miopía. Arch. Soco Ofta1. Hisp. Amer. 14, 116.
24. Barraquer, T. y Barraquer J., (956). Nueva Orientación Terapéutica en la Miopía Progresiva. Areh. Soe. Oftal. Hisp. Amer. 16, 1.137.
25. Barraquer, JI. Bases de la queratoplastia refractiva. Arch. Soc amer oftal. optom. (]965). 5 ·179.
26. Trokel SL, et al. Excimer Laser Radial Keratotomy. Ophthalmology 1985 Feb; 92 (2); 206-8.
27. Marshal J, Trokel S, Rothery S. A comparative study of corneal incisions induced by diamond and steel knives and two ultraviolet radiations from two excimer lasers. Br J of Ophthalmol. 70(7); 482-501.
28. Marshal J, Trokel S, Rothery S, Krueguer RR. Long term healing of the central cornea after photorefractive keratectomy using an excimer laser. Ophthalmology 1988. OCT; 95(10);1411-21.
29. Pallikaris IG, Papatzanaki ME, Stathi EZ, Frenschock O, Georgiadis A. Laser in situ keratomileusis. Laser in surgery and medicine. 1990; 10(5); 463-8.
30. MacDonalds MB, Conductive Keratoplasty: a radio frecquency-based technique for the correction of Hyperopia. Trans Am Ophthalmol Soc. 2005; 103:512-536.
31. Zaldivar R, Davidorf JM, Oscherow S. Posterior chamber Phakic intraocular lens for Myopia -8 to -19 Diopters. J Refract Surg 1998 May-Jun; 14(3): 294-305.
32. Zaldivar R, Davidorf JM, Oscherow S. Posterior chamber Phakic intraocular lens for Hyperopic +4 to +11 Diopters. J Refract Surg 1998 May-Jun; 14(3): 294-305.
33. Tsiklis NS, Kymions GD, Karp CL, Naomidi T, Pallikaris A. Nine-year follow-up of a posterior chamber phakic lens IOL in one eye and LASIK in a fellow eye of the same patient. J Refract Surg 2007 Nov; 23 (9): 935-7
34. Lee SY, et all. Comparison of patients outcomes after implantation of Visian toric Implantable Collamer Lens and iris fixated toric phakic intraocular lens. Eye 2011 Nov; 25 (11): 1409-17.
35. Zaldivar R, Oscherow S, Piezzi V. Bioptics in phakic and pseudopahkic intraocular lens with the NidekEC 5000 excimer lens. J Refract Surg 2002 May-Jun; 18(3):s336-9
36. Abell RG, Davies PE, Phelan D, Goemann K, McPherson ZE, Vote BJ. Anterior capsulotomy integrity after femtosecond laser-assisted cataract surgery. Ophthalmology. 2014 Jan;121(1):17-24.
37. Woodcock MG, Lehmann R, Cionni RJ, Breen M, Scott MC. Intraoperative aberrometry versus standard preoperative biometry and toric IOL calculator for bilateral toric IOL with femtosecond laser. J Cataract RefracT Surg 2016 Jun; 42 (6): 817-25.
38. Masket S, Fram NR, Holladay J. Influence of ophthalmic viscosurgical devices on intraoperative aberrometry. J Cataract Refract Surg 2016 Jul; 42 (7): 990-4.
39. Yesilirmak N, Palioura S, Culbertson W, Yoo SH, Donaldson K. Intraoperative Wavefront Aberrometry for Toric IOL placement in eyes with history of refractive surgery. J of refract Surg 2016 Jan 32 (1):69-70.
40. Adenwala A. Historia de la facoemulsificación. En: Ashok G, editor. Dominando la facodinámica. Herramientas, tecnologías e innovaciones. New Delhi: Jaypee Brothers; 2008. p. 3-10.
41. Kelman CD Symposium: Phacoemulsification. Summary of personal experience. Trans Am Acad Ophthalmol Otolaryngol. 1974 Jan-Feb;78(1): OP35-8.
42. Kelman CD Symposium: Phacoemulsification. Summary of personal experience. Trans Am Acad Ophthalmol Otolaryngol. 1974 Jan-Feb;78(1): OP5-13.
43. Hill DC, Sudhakar S, Hill CS, King TS, Scott IU, Ernst BB, Pantanelli SM Intraoperative aberrometry versus preoperative biometry for intraocular lens power selection in axial myopia. J Cataract Refract Surg. 2017 Apr;43(4):505-510. doi: 10.1016/j.jcrs.2017.01.014.
44. Schuster AK et all. Refractive, corneal and ocular residual astigmatism in a German population. Graefes Arch Clin Exp Ophthalmol 2017 dec 255 (12) 2493-2501.
45. De Medeiros AL, et al. Comparison of visual outcomes after bilateral implantation of a diffractive trifocal intraocular lens and blended implantation of an extended depth of focus lens with a diffractive bifocal IOL. Clin Ophthalmol 2017 Oct 26, 11: 1911-6.
46. Ruiz Mesa R, et al. Comparison of visual outcomes after bilateral implantation of extended range of vision and trifocal intraocular lenses. European Journal of Ophthalmol 2017 Jun 26; 27 (4) 460-5.
47. Ang et al. Refractive lenticule extraction: Transition and comparison of 3 surgical techniques Journal of Cataract & Refractive Surgery, Volume 40, Issue 9, 1415 – 1424.
48. Zaldivar R, Oscherow S, Piezzi V. Bioptics in phakic and pseudophakic intraocular lens with the Nidek EC-5000 excimer laser. J Refract Surg. 2002 May-Jun;18(3 Suppl):S336-9.
49. Zaldivar R, Davidorf JM, Oscherow S, Ricur G, Piezzi V. Combined posterior chamber phakic intraocular lens and laser in situ keratomileusis: bioptics for extreme myopia. J Refract Surg. 1999 May-Jun;15(3):299-308.
50. Velarde JI, Anton PG, de Valentin-Gamazo L Intraocular lens implantation and laser in situ keratomileusis (bioptics) to correct high myopia and hyperopia with astigmatism. J Refract Surg. 2001 Mar-Apr;17(2 Suppl): S234-7.
51. Malbran ES, et al Lens guide suture for transport and fixation in secondary IOL implantation after intracapsular extraction. Int Ophthalmol. 1986 May;9(2-3):151-60.
52. Norrby S Sources of error in intraocular lens power calculation. J Cataract Refract Surg 2008; Mar34(3) 368-76
Norrby et all Prediction of the true IOL position. Br J Ophthalmol. 2017 Oct; 101 (10): 1440-46.
53. Shammas J Biometry measurements using a new large-coherence–length swept-source optical coherence tomographer. J Cataract Refract Surg 2016 Jan; 42 (1) 50-61.
54. Mayer WJ, Klaproth OK, Hengerer FH, Kohnen T. Impact of crystalline lens opacification on effective phacoemulsification time in femtosecond laser-assisted cataract surgery. Am J Ophthalmol 2014; 157:426–432.
55. Haigis W Intraocular Lens calculation after refractive surgery for myopia. Haigis L Formula. JCRS 2008; 34 (10): 1658-1663.
56. Badoza D, Cosentino MJ, Moreno M, Lentes intraoculares tóricas en casos de catarata y ectasia corneal. Oftalmología Clínica y Experimental, 2015; 8(1): 1-8.
57. Gayton JL, Sanders VW. Implanting two posterior chamber intraocular lenses in a case of microphthalmos. J Cataract Refract Surg. 1993;19(6):776-777.
58. Gayton J, Sanders V, Van Der Karr M et al. Piggybacking Intraocular Implants to Correct Pseudophakic Refractive Errors. Ophthalmology. 1999; 106:56-59.
59. Habot-Wilner Z, Sachs D, Cahane M et al. Refractive results with secondary piggyback implantation to correct pseudophakic refractive errors. J Cataract Refract Surg. 2005; 31:2101-2103.
60. Alio, J, Rodriguez-Prats. Buscando la excelencia en la cirugía de catarata. Pág. 138.
61. Berck T, Shenkler M, Campos-Möller X, Pereira A, Ahmed I. Visual and refractive outcomes in manual vs femtosecond laser-assisted cataract surgery. Ophthalmology 2018. 1-9.
62. Hatch K, Schultz T, Talamo J, Burkhard D. Femtosecond laser-assisted compared with standard cataract surgery for removal of advanced cataracts. J Cataract Refract Surg 2015. 41: 1833-8.
